某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如图所示。据图判断正确的是
| A.Ⅱ为盐酸稀释时的pH值变化曲线 |
| B.b点溶液的导电性比c点溶液的导电性强 |
| C.a点KW的数值比c点KW的数值大 |
| D.b点酸的总浓度大于a点酸的总浓度 |
下列说法正确的是
| A.要实现低碳生活,必须停止使用所有燃料 |
| B.N和K都是植物生长的必需元素,因此可以将铵态氮肥和草木灰同时施用 |
| C.雾天行车要打开汽车大灯,这时若看到光路是由于“丁达尔现象” |
| D.硅是一种灰黑色的金属单质,是现代信息产业的重要元素 |
将2mol SO2和1mol O2充入一个容积固定的密闭容器中,在一定温度、催化剂作用下发生反应:2SO2(g)+O2(g)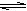 2SO3(g)。下列哪种量不再变化时,不能说明化学反应已经达到平衡状态的是
2SO3(g)。下列哪种量不再变化时,不能说明化学反应已经达到平衡状态的是
| A.混合气体的总物质的量 | B.混合气体的总压强 |
| C.SO2的转化率 | D.混合气体的密度 |
由氧化铜和氧化铁的混合物a g,加入2 mol·L-1的硫酸溶液50  mL,恰好完全溶解,若将a g的该混合物在过量的CO气流中加热充分反应,冷却后剩余固体的质量为
mL,恰好完全溶解,若将a g的该混合物在过量的CO气流中加热充分反应,冷却后剩余固体的质量为
| A.1.6a g | B.(a-1.6) g | C.(a-3.2) g | D.无法计算 |
下列各组单质中,前者能将后者从化合物中置换出来的是
①Al、Fe②C、Si③Mg、C④H2、Cu
A.只有①③ B.①②③④ C.只有②④ D.只有①②
常温时,下列各组离子在指定溶液中能大量共存的是
| A.pH = 1的溶液中: Fe2+、NO3-、SO42-、Na+ |
| B.c(Fe3+) =" 0.1" mol/L的溶液中:K+、ClO-、SO42-、SCN- |
| C.c(H+)/c(OH-) = 1012的溶液中: NH4+、Al3+、NO3-、Cl- |
| D.由水电离的c(H+) = 1×10-14 mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |