在一密闭容器中,反应aA(气) bB(气)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新平衡时,B的浓度是原来的40%,则( )
bB(气)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新平衡时,B的浓度是原来的40%,则( )
| A.平衡向正反应方向移动了 | B.物质A的转化率减小了 |
| C.物质B的质量分数增加了 | D.a< b |
在温度体积不变的条件下发生反应:NO2(g)+SO2(g)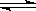 SO3(g)+NO(g)将NO2与SO2以体积比3:1置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
SO3(g)+NO(g)将NO2与SO2以体积比3:1置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
| A.混合气体密度保持不变 |
| B.体系压强保持不变 |
| C.SO2和NO的体积比保持不变 |
| D.每消耗1mol SO2的同时生成1molNO |
下列说法正确的是
| A.增大压强,活化分子百分数增多,化学反应速率一定增大 |
| B.升高温度,活化分子百分数不变,化学反应速率一定增大 |
| C.加入反应物,使活化分子百分数增大,化学反应速率增大 |
| D.使用催化剂,降低了反应的活化能,增大了活化分子百分数,化学反应速率一定增大 |
实验室用4 mol SO2与2 mol O2在一定条件下进行下列反应:2SO2(g)+O2(g)  2SO3(g) ΔH=-196.64 kJ/mol,当放出314.624 kJ热量时,SO2的转化率为
2SO3(g) ΔH=-196.64 kJ/mol,当放出314.624 kJ热量时,SO2的转化率为
| A.40% | B.50% | C.80% | D.90% |
用纯净的CaCO3与稀盐酸反应制取CO2,实验过程记录如图所示。根据分析、判断,正确的是 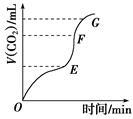
| A.OE段表示反应速率最快 |
| B.EF段表示反应速率最快,单位时间内收集的CO2最多 |
| C.FG段表示收集的CO2最多 |
| D.OG段表示随着时间的推移,反应速率逐渐增快 |
在2 L容器中发生3A+B  2C的反应,最初加入的A、B都是4 mol,若10 s 后反应达到平衡,测得A的平均反应速率为0.15 mol·L-1·s-1,则10 s后容器内B的物质的量为
2C的反应,最初加入的A、B都是4 mol,若10 s 后反应达到平衡,测得A的平均反应速率为0.15 mol·L-1·s-1,则10 s后容器内B的物质的量为
A.1.5 molB.1.0 mol C.3.0 molD.2.4 mol