(共12分)配制250mL 1.0mol/L NaOH溶液,请回答下列问题:
⑴在下列仪器中:A 托盘天平 B 量筒 C烧杯 D 玻璃棒 E 漏斗 F 500mL容量瓶
G 药匙 H 250mL容量瓶 I 胶头滴管 J 坩埚
需要用到的仪器有
⑵所需NaOH固体质量为 克
⑶配制的实验步骤如下:
①计算 ②称量 ③溶解 ④转移、洗涤 ⑤定容 ⑥摇匀
其中第③、④、⑤步实验操作都要用到玻璃棒,作用分别是 , ,
。
⑷在容量瓶内确定溶液体积的过程中,完成后期加入少量水的做法是
;
下列各项中,可能导致实际浓度偏高的是 (填标号)
| A.在天平托盘上垫纸,将NaOH放在纸上称量 |
| B.NaOH溶解时放出大量的热,未冷却立即配制溶液 |
| C.溶解NaOH固体之后的烧杯未洗涤 |
| D.向容量瓶中转移液体时不慎洒出 |
⑸从上述所配制的溶液中取出10mL,其中NaOH的物质的量浓度为 ,NaOH的质量为 ,NaOH的物质的量为 。
⑹将取出的10mL溶液加水稀释到100mL,稀释后溶液中N aOH的物质的量浓度为 。
aOH的物质的量浓度为 。
下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题:
| 族 周期 |
IA |
0 |
||||||
| 1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 2 |
② |
③ |
④ |
|||||
| 3 |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
(1)元素②在周期表中的位置是
(2)在①~⑨元素中,金属性最强的元素是,非金属性最强的元素是。(均填元素符号)
(3)元素⑦与元素⑧相比,⑧的非金属性较强,下列表述中能证明这一事实的是
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
d.⑦的氧化物的水化物比⑧的氧化物的水化物酸性弱
设计一个简单实验,证明元素⑦与元素⑧的非金属性强弱,请写出反应的化学方程式__________
(4)⑤与⑥两元素最高价氧化物的水化物相互反应的化学方程式为____________________
(5)③的氢化物的电子式为__________________
①④⑤三种元素形成的最简单一种化合物含有的化学键类型有
把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题: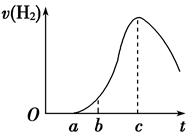
(1)曲线由O →a段不产生氢气的原因是___________________________________
有关反应的化学方程式为_________________________________
(2)曲线a→c段,产生氢气的速率增加较快的主要原因是_________________________
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因是_________________________
(4)该反应若使用催化剂,可使H2产量增多吗______________(填“会”或“不会”)。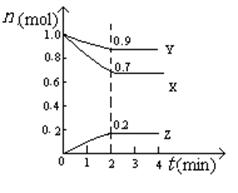
(5)某温度时,在2L密闭容器中X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。
由图中的数据分析,该反应的化学方程式为。
反应从开始至2min末,Z的平均反应速率为。
(Ⅰ)下列装置能组成原电池的是_____________ (填序号)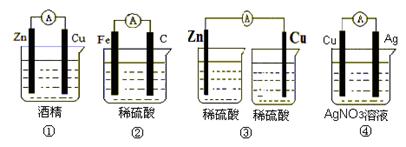
(Ⅱ)如上图④所示,若是原电池,请回答下列问题(若不是原电池,则不用回答)。
(1)负极材料是_______________________
(2)正极的电极反应式为________________________
(3)电池工作时总反应的离子方程式是____________________________
(4)导线中电子的流向________________________________
(5)阳离子的移动方向___________________________________
(6)该装置将能转化为能。
黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe2O3。
(1)将0.050mol SO2(g)和0.030mol O2(g)放入容积为1L的密闭容器中,反应:
2SO2(g)+O2(g) 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol·L-1。计算该条件下反应的平衡常数K和SO2的平衡转化率、。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol·L-1。计算该条件下反应的平衡常数K和SO2的平衡转化率、。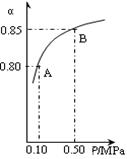
(2)已知上述反应是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的有(填字母序号,多选倒扣分)。
A.升高温度B.降低温度
C.增大压强D.加入催化剂
E.移出氧气
(3)某温度下,上述反应中SO2的平衡转化率(α)与体系总压强(p)的关系如右图所示。判断:平衡状态由A变到B时,平衡常数K(A)______K(B)(填“>”、“<”或“=”)。
(1)土壤的pH一般在4~9之间。土壤中Na2CO3含量较高时,pH可以高达10.5,试用离子方程式解释土壤呈碱性的原因;加入石膏(CaSO4 2H2O)可以使土壤碱性降低,有关反应的化学方程式为。
2H2O)可以使土壤碱性降低,有关反应的化学方程式为。
(2)在一定条件下进行如下反应:aX(g)+bY(g) cZ(g)
cZ(g)
右图是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强关系示意图。
① 写出该反应的化学平衡常数表达式:K=。随着温 度的升高,K值(填“增大”、“减小”或“不变”)。当反应物起始浓度相同时,平衡常数K值越大,表明(字母填序号)。
| A.X的转化率越高 | B.反应进行得越完全 |
| C.达到平衡时X的浓度越大 | D.化学反应速率越快 |
② 如右图所示,相同温度下,在甲、乙两容器中各投入1molX、2molY和适量催化剂,甲乙两容器的初始体积均为1L,甲、乙容器达到平衡所用时间:甲乙(填“>”、“<”或“=”,下同),平衡时X和Y的转化率:甲乙。