下列离子方程式正确的是( )
A.用铂电极电解氯化镁溶液:2Cl-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
| B.向NaHS溶液中通入过量氯气:HS-+Cl2=S↓+H++2Cl- |
C.向Fe(OH)3悬浊液中加入氢碘酸:Fe(OH)3+3H+= Fe3++3H2 O O |
| D.用醋酸除去水垢:CaCO3+2H+=Ca2++H2O+CO2↑ |
.有关实验方法和解释或结论都正确的是的
| 实验方法 |
解释或结论 |
|
| A |
高级脂肪酸甘油酯中加人NaOH溶液,加热后不再分层 |
皂化反应进行完全 |
| B |
将苯滴人溴水中,振荡后溴水层褪色 |
苯与溴发生了加成反应 |
| C |
用蘸浓氨水的玻璃棒放于试剂瓶口,有大量白烟 |
该试剂一定为盐酸 |
| D |
用标准Na0H溶液滴定未知酸液,逐滴滴至溶液刚好变红 |
达到滴定终点 |
.氯磺酸(HSO3C1)是一种容易水解的一元强酸,可以在常温下用HCl+SO3=HSO3Cl制得,
下列说法正确的是
| A.HS03Cl与H20反应产物为H2S04和HCl |
| B.HSO3Cl与NaOH溶液反应生成产物只有NaS03Cl |
| C.HSO3Cl也可以用浓盐酸与浓硫酸反应制得 |
| D.O.1mol的HSO3Cl与HCl分别溶于水制得1L溶液,两者pH都等于1 |
.如图所示是制备药物氧氟沙星的中间体,它不能发生的反应类型是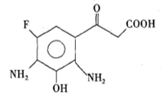
| A.加成反应 | B.取代反应 |
| C.水解反应 | D.加聚反应 |
.甲醛是一种重要的化工产品,可以利用甲醇脱氢制备,反应式如下:
①CH30H(g)=CH20(g)+H2(g)△H1=+84.2kJ·mol-1
向反应体系中通入氧气,通过反应②2H2(g)+O2(g)=2H2O(g)△H2="-483.6" kJ·mol-1提供反应①所需热量,要使反应温度维持在700°c,则进料中甲醇与氧气的物质的量之比为
| A.5.74:1 | B.11.48:1 | C.1:l | D.2:l |
.下列对有关化学反应过程或实验现象的解释中,正确的是
| A.NH3的水溶液可以导电,说明NH3是电解质 |
| B.在高温条件下,C能置换出SiO2中的Si,说明C的氧化性强于Si。 |
| C.在滴有酚酞的Na2CO3溶液中,加入CaCl2溶液,溶液褪色,说明CaCl2溶液有酸性 |
| D.向淀粉碘化钾的溶液中加入溴水,溶液变为蓝色,说明Br2的氧化性强于I2 |