高温下,某反应达平衡,平衡常数 ,恒容时,温度升高,H2浓度减小。下列说法正确的是
,恒容时,温度升高,H2浓度减小。下列说法正确的是
| A.该反应的焓变为正值 |
B.恒温恒 容下,增大压强,H2浓度一定减小 容下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 |
D.该反应的化学方程式为 CO + H2O CO2 + H2 CO2 + H2 |
下图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是()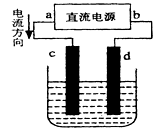
| A.a为负极、b为正极 |
| B.d为阳极,电极反应为:2Cl—-2e—=Cl2↑ |
| C.电解过程中,d电极质量增加 |
| D.电解过程中,氯离子浓度不变 |
已知N2(g)+3H2(g)  2NH3(g),现向一密闭容器中充入1molN2和3molH2,在高温、高压和催化剂存在条件下发生反应。下列有关说法正确的是()
2NH3(g),现向一密闭容器中充入1molN2和3molH2,在高温、高压和催化剂存在条件下发生反应。下列有关说法正确的是()
| A.最终可以生成2mol NH3 |
| B.达到化学平衡状态时,正反应和逆反应的速率都为0 |
| C.达到化学平衡状态时,容器中N2、H2和NH3的物质的量之比为1∶3∶2 |
| D.达到化学平衡状态时,N2、H2和NH3的物质的量浓度不再变化 |
下图为番茄电池,下列说法正确的是()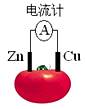
| A.一段时间后,锌片质量会变小 | B.铜电极附近会出现蓝色 |
| C.电子由铜通过导线流向锌 | D.锌电极是该电池的正极 |
用铁片与稀硫酸反应制取氢气时,下列措施中,不能使氢气生成速率加快的是()
| A.加热 | B.不用稀硫酸,改用98%浓硫酸 |
| C.滴加少量CuSO4溶液 | D.不用铁片,改用铁粉 |
已知An+、B(n-1)+、C(n+1)+、D(n+1)-都有相同的电子层结构,A、B、C、D的原子半径由大到小的顺序是()
A.C>D>B>AB.A>B>C>D C.B>A>C>D D.A>B>D>C