科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)用太阳能分解10mol液态水消耗的能量是__________kJ;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为________________________________;
(3)在容积为2L的密闭容器中,由一定量的CO2和H2合成甲醇,在其他条件不变的情况下,温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);下列说法正确的是___________(填序号)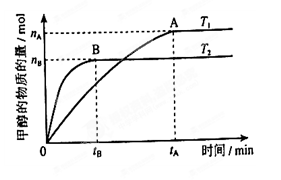
① 温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=  mol·L-1·min-1
mol·L-1·min-1
② 该反应在T1时的平衡常数比T2时的大
③ 该反应的 △H < 0
④ 处于A点的反应体系从T1变到T2,达到平衡时容器中气体密度减小
⑤处于A点时容器中的压强比处于B点时容器中的压强大
(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a, 则容器内的压强与起始压强之比为___________;
(5)在直接以甲醇为燃料的电池中,电解质溶液为酸性,负极的反应式为________________________。
下列说法中正确的一组是()
| A.H2和D2互为同位素 |
B.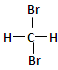 和 和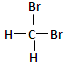 互为同分异构体 互为同分异构体 |
| C.正丁烷和异丁烷是同系物 |
D.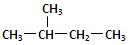 和 和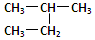 是同一种物质 是同一种物质 |
下列说法正确的是
①离子化合物含离子键,也可能含极性键或非极性键
②共价化合物含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥熔融状态能导电的化合物是离子化合物
| A.①③⑥ | B.②④⑥ | C.②③④ | D.①③⑤ |
某烷烃的一种同分异构体只能生成一种一氯代物,则其分子式不可能是( )
| A.C2H6 | B.C4H10 | C.C5H12 | D.C8H18 |
下列化学用语正确的是( )
A.CH4分子的球棍模型: |
B.乙烯的结构简式:CH2CH2 |
C.钙离子的结构示意图: |
D.聚丙烯的结构简式: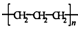 |
下列反应中,属于氧化还原反应同时又是吸热反应的是()
| A.Ba(OH)2·8H2O与NH4Cl反应 | B.铝与稀盐酸 |
| C.灼热的炭与CO2反应 | D.甲烷与O2的燃烧反应 |