铝分别与足量的稀盐酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗 的HCl和NaOH物质的量之比为
的HCl和NaOH物质的量之比为
| A.1 : 1 | B.2 : 1 | C.3 : 1 | D.1 :3 |
下图是某同学做完Zn-Cu原电池实验后所做的读书卡片记录,在卡片上,描述合理的是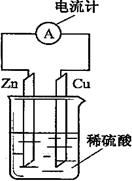

| A.①③ | B.①④ | C.②③ | D.③④ |
下列装置能达到实验目的的是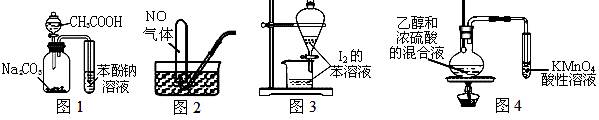
| A.图1证明酸性:CH3COOH>H2CO3>苯酚 | B.图2用排水法收集NO |
| C.图3萃取碘水中I2,分出水层后的操作 | D.图4验证乙烯的生成 |
下列实验操作、现象和结论均正确的是
| 选项 |
实验操作 |
现象 |
结论 |
| A. |
向AgCl悬浊液中加入稀的NaI溶液 |
出现黄色沉淀 |
Ksp(AgCl)>Ksp(AgI) |
| B. |
在某溶液中加KSCN |
溶液显红色 |
该溶液中有Fe3+,无Fe2+ |
| C. |
在酒精灯上加热铝箔 |
铝箔熔化滴落下来 |
金属铝的熔点较低 |
| D. |
将气体通入澄清石灰水 |
溶液变浑浊 |
该气体一定是CO2 |
下列关于有机化合物的说法正确的是
| A.聚乙烯分子中含碳碳双键 | B.油脂的皂化反应属于加成反应 |
| C.丁烷有3种同分异构体 | D.以淀粉为原料可以制备乙醇 |
下列有关化学用语表达正确的是
A.HCl的电子式: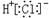 |
B.氯离子(Cl-)的结构示意图: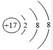 |
| C.乙酸的结构简式:C2H4O2 | D.质子数为17、中子数为20的氯原子: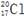 |