将一定量的SO2和氧气放入一定体积的密闭容器中,550 ℃时,在催化剂作用下发生反应:2SO2(g)+O2(g) 2SO3(g)(正反应放热)。判断该反应达到平衡状态的标志是( )
2SO3(g)(正反应放热)。判断该反应达到平衡状态的标志是( )
| A.SO3的生成速率与SO2的消耗速率相等 |
| B.SO3的浓度等于SO2的浓度 |
C.容器 中气体的压强不变 中气体的压强不变 |
| D.容器中混合气体的密度保持不变 |
有机物甲用质谱仪测定如图1,核磁共振氢谱示意如图2,则甲的结构简式可能为

| A.HCOOH | B.CH3CHO | C.CH3CH2OH | D.CH3CH2CH2COOH |
下列与键线式为 的物质互为同分异构体的是
的物质互为同分异构体的是
A. |
B. |
C.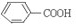 |
D. |
按系统命名法给下列有机物命名正确的是
A.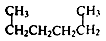 1,4-二甲基丁烷 1,4-二甲基丁烷 |
B.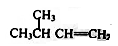 3-甲基丁烯 3-甲基丁烯 |
C. 2-甲基丁烷 2-甲基丁烷 |
D.CH2Cl-CH2Cl二氯乙烷 |
下列关于有机物的说法不正确的是
| A.可用水来鉴别苯和CCl4 |
| B.煤的干馏属于化学变化,硝化反应、酯化反应、皂化反应都属于取代反应 |
| C.CH2Cl2有两种同分异构体 |
| D.高温加热能杀死病毒是因为构成病毒的蛋白质受热变性 |
有机化合物与我们的生活息息相关,下列说法正确的是
| A.淀粉和纤维素的分子式都为(C6H10O5)n,所以淀粉和纤维素互为同分异构体 |
| B.蛋白质水解生成葡萄糖并放出热量,提供生命活动的能量 |
| C.糖类、油脂、蛋白质都属于天然高分子化合物 |
| D.低级酯具有芳香气味,日常生活中的饮料、糖果盒糕点等常使用低级酯作香料 |