NA表示阿伏加德罗常数,下列说法正确的是
| A.标准状况下,等体积的水和CO2,含有的氧原子数目为1∶2 |
| B.含有NA个阴离子的Na2O2与足量水反应,转移电子数为2NA |
| C.向FeI2溶液中通入适量氯气,当有NA个Fe2+被氧化时,共转移电子数为3NA |
| D.一个NO分子质量为a g,一个NO2分子质量是b g,则NA个O2的质量为(b—a)NAg |
下列有关试剂的保存方法,错误的是()
| A.氢氧化钠溶液保存在具有橡胶塞的广口玻璃试剂瓶中 |
| B.新制的氯水通常保存在棕色玻璃试剂瓶中 |
| C.少量的钠保存在煤油中 |
| D.浓硝酸保存在棕色玻璃试剂瓶中 |
下列材料一定不属于天然材料的是()
| A.纤维素 | B.金刚石 | C.聚乙烯 | D.油脂 |
实验室在配制硫酸铁溶液时,先把硫酸铁晶体溶解在稀硫酸中,再加水稀释至所需浓度,如此操作的目的是()
| A.防止硫酸铁分解 | B.抑制硫酸铁水解 |
| C.提高硫酸铁的溶解度 | D.提高溶液的pH值 |
某有机物结构为: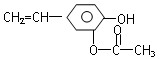 ,它可能具有的性质是()
,它可能具有的性质是()
①能使KMnO4酸性溶液褪色②能与NaOH溶液反应
③能发生聚合反应④能与Ag(NH3)2OH溶液发生银镜反应
| A.只有①② | B.只有②③ | C.只有①②③ | D.①②③④ |
下列过程合乎实际并用于工业生产的是()
| A.钠在氯气中燃烧制氯化钠 | B.氯化铵与氢氧化钙共热制氨气 |
| C.浓盐酸与二氧化锰共热制氯气 | D.氯气与石灰乳反应制漂白粉 |