下列除去杂质的方法正确的是
| A.除去CO2中混有的CO:将混合气体通过装有NaOH溶液的洗气瓶 |
| B.除去铜器表面的铜绿:用稀硝酸浸泡,再用水冲洗 |
| C.除去KNO3溶液中少量NaCl:加水溶解,蒸发结晶,趁热过滤 |
| D.除去Mg(OH)2固体中少量Ca(OH)2:加入足量MgCl2溶液,充分搅拌后过滤 |
下列说法正确的是( )
| A.纤维素属于髙分子化合物,与淀粉互为同分异构体,水解后均生成葡萄糖 |
B.某有机物结构如图所示,该有机物属于芳香族化合物的同分异构体有5种,其中遇FeCl3溶液能显色的有3种 |
| C.5个碳原子的有机物,每个分子中最多可形成4个碳碳单键 |
| D.2,3二甲基丁烷的H—NMR上有5个峰 |
下列叙述不正确的是( )
| A.金刚石、碳化硅、晶体硅的熔点依次降低 |
| B.CaO晶体结构与NaCl晶体结构相似,每个CaO晶胞中含有4个Ca2+和4个O2- |
C.设NaCl的摩尔质量为M g·mol-1,NaCl的密度为ρ g·cm-3,阿伏加德罗常数为NA mol-1,在NaCl晶体中,两个距离最近的Cl-中心间的距离为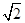 · ·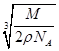 cm cm |
| D.X、Y可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角位置,则该晶体的组成式为XY3 |
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示。常温下,S2Cl2是一种橙黄色液体,遇水易水解,并产生能使品红褪色的气体, 化学方程式为2S2Cl2+2H2O=SO2↑+3S↓+4HCl。下列说法中错误的是( )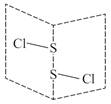
| A.S2Cl2的结构式为Cl—S—S—Cl |
| B.反应中SO2是还原产物,S是氧化产物 |
| C.S2Cl2为含有极性键和非极性键的分子 |
| D.S原子采取sp3杂化 |
下列有关元素锗及其化合物的叙述中正确的是( )
| A.锗的第一电离能高于碳而电负性低于碳 |
| B.四氯化锗与四氯化碳分子都是四面体构型 |
| C.二氧化锗与二氧化碳都是非极性的气体化合物 |
| D.锗和碳的单质都是原子晶体 |
海水淡化的方法有多种,如蒸馏法、电渗析法等。电渗析法是一种利用离子交换膜进行离子交换的方法,其原理如图所示。已知海水中含Na+、Cl-、Ca2+、Mg2+、SO等离子,电极为惰性电极。下列叙述中正确的是( )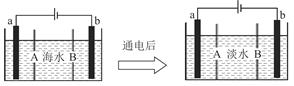
| A.B膜是阴离子交换膜 |
| B.通电后,海水中阳离子向a电极处运动 |
| C.通电后,a电极的电极反应式为4OH--4e-=O2↑+2H2↑ |
| D.通电后,b电极上产生无色气体,溶液中出现少量白色沉淀 |