某无色混合盐溶液中,除水电离产生的离子外可能含有①Na+ ②Ba2+ ③Cl— ④Br—⑤SO32— ⑥SO42—离子中的若干 种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
| 步骤 |
操作 |
现象 |
| (1) |
用pH试纸检验 |
溶液的pH大于7 |
| (2) |
向溶液中滴加氯水,再加入CCl4振荡,静置 |
CCl4层呈橙色 |
| (3) |
分液,向 所得水溶液中加入Ba(NO3) 2溶液和稀HNO3 所得水溶液中加入Ba(NO3) 2溶液和稀HNO3 |
有白色沉淀产生 |
| (4) |
过滤,向滤液中加入AgNO3溶液和稀HNO3 |
有白色 沉淀产生 沉淀产生 |
下列结论正确的是( )
A.肯定含有的离子是①④⑤ B.肯定没有的离子是②⑥
C.不能确定的离子是① D.只能确定④存在,②不存在
2008年奥运会将在北京举行,这届奥运会吉祥物五个福娃已经被做成各种玩具,有一种玩具的内充物为无毒的聚酯纤维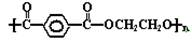 ,下列说法正确的是()
,下列说法正确的是()
| A.聚酯纤维是高分子化合物,是一种纯净物 |
| B.聚酯纤维一定易溶于水 |
| C.聚酯纤维可能易着火 |
| D.由单体合成聚酯纤维的反应属加聚反应 |
已知分子式为C10H14的烃,其一溴代物的同分异构体有四种,则该烃的结构简式可能是()
下列烷烃的名称正确的是()
A.2-甲基-4-乙基庚烷 B.1,2-二甲基戊烷
B.2-乙基丁烷D.2,3-二乙基-4-甲基己烷
用分液漏斗可以分离的一组是()
| A.碘和乙醇 | B.溴苯和水 | C.甘油和水 | D.甲醇和甘油 |
下列关于烃的说法中,正确的是()
A.烃是指分子里含有C元素的化合物
B.烃是指分子里含有C、H元素的化合物
C.烃是指仅由C和H两种元素组成的化合物
D.烃是指燃烧反应后生成CO2和H2O的有机物