下列叙述正确的是( )
| A.1 mol H2O的质量为18g/mol | B.CH4的摩尔质量为16g |
| C.3.01×1023个SO2分子的质量为32g | D.标准状况下,1 mol任何物质体积均为22.4L |
下列有关化学实验的叙述不正确的是:()
| A.用托盘天平称量氢氧化钠固体时,应将药品放在烧杯中称量 |
| B.中和热的测定试验中,若用弱酸代替强酸做实验,会导致反应产生的热量少 |
| C.为抑制硫酸亚铁溶液中Fe2+的水解,可加稀硝酸酸化 |
| D.用PH试纸检测溶液的PH值时,用洁净干燥的玻棒蘸取溶液,点在试纸上,再与标准比色卡比色 |
在pH=1的溶液中能大量共存的一组离子是
| A.Na+、Mg2+、ClO—、NO3— | B.Al3+、NH4+、Br—、SO42— |
| C.K+、Fe3+、SO32—、HCO3— | D.Na+、K+、SiO32—、Cl— |
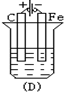
下列各烧杯中均盛着海水,其中铁腐蚀最快的是


对于反应2X(g)+Y(g) 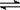 2Z(g),下列说法正确的是
2Z(g),下列说法正确的是
| A.由于K=CZ2/(CX2CY),随着反应的进行,Z的浓度不断增大,X,Y的浓度不断减小,平衡常数不断增大 |
| B.当温度不变时,增大反应物的浓度,使K变小;增大生成物的浓度,使K增大 |
| C.可逆反应达到平衡时,逆反应便立即停止了 |
| D.温度发生变化,上述的K值也发生变化 |
13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,Kurt Wuithrich等人为此获得2002年诺贝尔化学奖。下面有关13C、15N的叙述正确的是
A.13C与15N有相同的中子数 B.13C电子排布式为1s22s22p3
C.15N与14N互为同位素 D.15N的电子排布式为1s22s22p4