某学习小组根据化学知识和下表的数据,设计了表中的实验,以验证酸性:盐酸>碳酸>苯酚>碳酸氢根离子,其中不合理的是 ( )
| 物质 |
电离常数 |
和溶解度(25℃) |
| C6H5OH |
K=1.28×10-10 |
S = 9.3g/100g水 |
| H2CO3 |
K1 =4.3×10-7 |
|
| K2 =5.6×10-11 |
|
| |
组别 |
操作 |
判断依据 |
| A |
盐酸和碳酸 |
往碳酸钙固体中滴加盐酸 |
观察有无气体产生 |
| B |
碳酸与苯酚 |
往苯酚钠饱和溶液中,通入足量CO2 |
观察溶液是否变浑浊 |
| C |
碳酸与苯酚 |
配制同物质的量浓度的碳酸钠溶液和苯酚钠溶液 |
比较溶液的pH |
| D |
HCO3-与苯酚 |
在苯酚悬浊液中,加入过量的 Na2CO3溶液 |
观察悬浊液是否变澄清 |
下列电子式书写正确的是()
A. |
B. |
C. |
D. |
短周期的两种元素A和B,它们的离子A-和B2+具有相同的电子层结构,下列说法中正确的是:( )
| A.原子序数A>B | B.电子总数A>B | C.离子半径A->B2+ | D.原子半径A>B |
下列物质的性质比较,正确的是:( )
| A.酸性:H2SO4>HClO4>HBrO4 | B.碱性:NaOH>KOH>RbOH |
| C.非金属性: P>S>Cl | D.气态氢化物稳定性:HF>HCl>H2S |
已知R2+离子核外有a个电子,b个中子。表示R原子符号正确的是( )
A. |
B. |
C. |
D. |
下列说法正确的是()
| A.NaCl固体中含有共价键 |
| B.CO2分子中含有离子键 |
C. 、 、 、 、 是碳的三种核素 是碳的三种核素 |
D.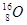 、 、 、 、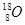 含有相同的中子数 含有相同的中子数 |