某学生配制一定物质的量浓度的氢氧化钠溶液后,经测定发现溶液浓度偏低。该学生找出以下原因,其中不会使溶液浓度偏低的是
| A.没有用蒸馏水洗烧杯2—3次,并将洗液移入容量瓶中 |
| B.容量瓶刚用蒸馏水洗净,没有烘干 |
| C.定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切 |
| D.定容时仰视刻度线 |
下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O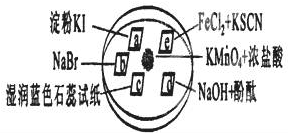
对实验现象的“解释或结论”正确的是
| 选项 |
实验现象 |
解释或结论 |
| A |
a处变蓝,b处变红棕色 |
氧化性:Cl2>Br2>I2 |
| B |
c处先变红,后褪色 |
氯气与水生成了酸性物质 |
| C |
d处立即褪色 |
氯气与水生成了漂白性物质 |
| D |
e处变红色 |
还原性:Fe2+>Cl- |
当光速通过下列分散系时,能产生丁达尔效应的是
| A.NaCl溶液 | B.泥水 | C.盐酸 | D.氢氧化铁胶体 |
下列各组离子中,在碱性溶液中能大量共存,且溶液为无色透明的是
| A.K+ MnO4- Cl- SO42- | B.Na+ AlO2- Cl-SO42- |
| C.SO42-Na+HCO3-Ba2+ | D.Na+ NO3- NH4+ SO42- |
下列是一些实验操作的示意图,其中不正确的是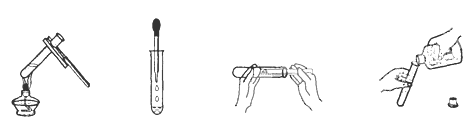
ABCD
为了检验某FeCl2溶液是否变质,可向溶液中加入
| A.氯水 | B.铁片 | C.KSCN溶液 | D.石蕊溶液 |