实验室用固体烧碱配制480mL 1mol/L NaOH溶液。
(1)需称量 g的烧碱固体,固体应放在 中称量。
(2)配制过程中,不需要使用的仪器是(填写代号 ) 。
) 。
A 烧杯 B 量筒 C 1000mL容量瓶 D 玻璃棒
1000mL容量瓶 D 玻璃棒
E 漏斗 F 胶头滴管 G 500mL试剂瓶
(3)根据实验的实际需要和(2)中列出的仪器判断,完成实验还缺少的仪器是 ;
(4)在定容的过程中,后期加入少量水的做法是 。
固体硝酸盐加热易分解且产物较复杂。某学习小组以Mg(NO3)2为研究对象,拟通过实验探究其热分解的产物,提出如下4种猜想:
甲:Mg(NO3)2、NO2、O2
乙:MgO、NO2、O2
丙:Mg3N2、O2
丁:MgO、NO2、N2
(1)实验前,小组成员经讨论认定猜想丁不成立,理由是。
查阅资料得知:2NO2+2NaOH=NaNO3+NaNO2+H2O
针对甲、乙、丙猜想,设计如下图所示的实验装置(图中加热、夹持仪器等均省略):
(2)实验过程
①取器连接后,放人固体试剂之前,关闭k,微热硬质玻璃管(A),观察到E 中有气泡连续放出,表明。
②称取Mg(NO3)2固体3.79 g置于A中,加热前通人N2以驱尽装置内的空气,其目的是;关闭K,用酒精灯加热时,正确操作是先然后固定在管中固体部位下加热。
③观察到A 中有红棕色气体出现,C、D 中未见明显变化。
④待样品完全分解,A 装置冷却至室温、称量,测得剩余固体的质量为1.0g⑤ 取少量剩余固体于试管中,加人适量水,未见明显现象。
(3)实验结果分析讨论
①根据实验现象和剩余固体的质量经分析可初步确认猜想是正确的。
②根据D 中无明显现象,一位同学认为不能确认分解产物中有O2,因为若有O2,D中将发生氧化还原反应:(填写化学方程式),溶液颜色会退去;小组讨论认定分解产物中有O2存在,未检侧到的原因是。
③小组讨论后达成的共识是上述实验设计仍不完善,需改进装里进一步研究。
利用酸解法制钛白粉产生的废液[含有大量FeSO4、H2SO4和少量Fe2(SO4)3TiOSO4],生产硫酸亚铁和补血剂乳酸亚铁。其生产步骤如下:
请回答:
(1)步骤①中分离操作的名称是______;步骤⑥必须控制一定的真空度,原因是_________;
(2)废液中的TiOSO4在步骤①能水解生成滤渣(主要成分为TiO2•xH2O)的化学方程式为__________;步骤④的离子方程式为_____________________。
(3)用平衡移动原理解释步骤⑤中加乳酸能得到乳酸亚铁的原因_______。
(4)配平酸性高锰酸钾溶液与硫酸亚铁溶液反应的离子方程式:_____Fe2++_____MnO4-+_____H+=_____Fe3++_____Mn2++_____
取步骤②所得晶体样品ag,溶于稀硫酸配成100.00 mL溶液,取出20. 00 mL溶液,用KMnO4溶液滴定(杂质与KMnO4不反应)。若消耗0.1000 mol·L-1KMnO4溶液20.00mL,则所得晶体中FeSO4•7H2O的质量分数为(以含a的式子表示)_____________________。
某校学生化学实验小组,为验证非金属元素氟的氧化性强于硫和氮,设计了一套实验装置:(部分加持装置已略去)
(1)写出A中反应的离子方程式。
(2)B中出现黄色浑浊现象,产生此现象的离子方程式。
(3)试从原子结构角度解释氯的氧化性大于硫的原因。
(4)D中干燥管中出现的现象及化学方程式。
(5)有同学认为D中的现象并不能说明氯的氧化性大于氮,需要在C之前加装洗气装置,请画出其装置图(并注明盛装试剂)。
(6)还有什么方法能证明氧化性Cl2>S,用一种相关事实说明。
某研究性学习小组通过下列实验探究SO2能否与BaCl2溶液反应生成BaSO3沉淀,并制备硫酸铜晶体。完成下列填空。甲同学用装置I进行实验,加热反应物至沸腾,发现BaCl2溶液中出现白色沉淀,且白色沉淀不溶于盐酸。
(1)白色沉淀是。
(2)甲同学就白色沉淀的生成原因提出了两种假设,这两种假设可能是:
①②
乙同学设计了改进装置Ⅱ进行实验,检验甲同学提出的假设(夹持装置和A中加热装置已略,气密性已检验)。
①打开弹簧夹,通入N2一段时间后关闭弹簧夹;
②滴加一定量浓硫酸,加热A,一段时间后C中未见沉淀生成。
(3)操作①的目的是,集气瓶B中的试剂是。
(4)该实验能否检验甲同学上述两种假设中的任意一种,理由是。
丙同学向反应后的蓝色溶液中加入足量的CuO,过滤后将滤液制成硫酸铜晶体(CuSO4·xH2O),采用加热法测定该晶体中结晶水x的值,实验数据记录如下:
| 坩埚质量 |
坩埚与晶体总质量 |
加热后坩埚与固体总质量 |
|
| 第一次称量 |
第二次称量 |
||
| 11.710g |
22.700g |
18.621g |
a |
(5)若无需再进行第三次称量,则a的数值范围应为。
(6)若加热后坩埚与固体总质量为18.620g,计算x 的实测值(保留二位小数),相对误差。
我国化工专家侯德榜,勇于创新,改进氨碱法设计了“联合制碱法”,为世界制碱工业作出了突出贡献。请完成下列问题:
(1)“联合制碱法”制得的“碱”是(填化学式)。
(2)氨碱法和联合制碱法是两大重要的工业制碱法,下列表达中,不正确的是。
| 氨碱法 |
联合制碱法 |
||
| A |
原料 |
食盐、氨气、生石灰 |
食盐、氨气、二氧化碳 |
| B |
可能的副产物 |
氯化钙 |
氯化铵 |
| C |
循环物质 |
氨气、二氧化碳 |
氯化钠 |
| D |
评价 |
原料易得;设备复杂;能耗高 |
原料利用率高;废弃物少 |
某实验小组,利用下列装置模拟“联合制碱法”。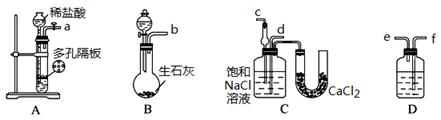
(3)取上述仪器连接装置,顺序为:(a)接()、()接();(b)接();
检验气密性后装入药品,应该先让装置(填上述字母)先发生反应,直到产生的气体不能再在C中溶解时,再通入另一装置中产生的气体。
(4)C中用球形干燥管而不用直导管,其作用是,D中应选用的液体为;
(5)C中广口瓶内产生固体的总化学方程式为。
(6)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为:(注明你的表达式中所用的有关符号的含义)。