设NA代表阿伏加德罗常数,下列说法正确的是( )
| A.常温常压下,氧气和臭氧的混合物16g中含有NA个氧原子 |
| B.标准状况下,11.2 LH2O中含分子数为0.5NA |
| C.标准状况下,22.4 LH2中含质子数为NA |
| D.100mL0.1mol·L-1的AlCl3溶液中含有Al3+的个数为0.01 NA |
向下列饱和溶液中加入少量物质后,原溶液不可能变浑浊的是
| 饱和溶液 |
加入的少量物质 |
|
| A |
NaHCO3 |
石灰水 |
| B |
盐酸 |
氢氧化钠溶液 |
| C |
Na2CO3 |
CO2 |
| D |
Ca(OH)2 |
CaCl2 |
下列各离子组在指定的溶液中一定能够大量共存的是
| A.在无色的溶液中:K+、Na+、MnO4-、SO42- |
| B.在pH=11的溶液中:CO32-、Na+、NO3-、SO42- |
| C.水电离出的c(H+)= 10-12 mol·L‾1的溶液中:Cl- 、HCO3-、NO3-、NH4+ |
| D.加入铝单质能放出氢气的溶液中:Mg2+、NH4+、Cl-、K+ |
下列装置及实验与结论对应正确的是
下列有关物质的性质、用途相对应都正确的是
| A.氯气具有还原性,可用于自来水的消毒杀菌 |
| B.水晶是无色透明的晶体,可用制作硅太阳能电池 |
| C.常温下铝在浓硫酸中钝化,常温下可用铝制容器盛放浓硫酸 |
| D.氨气可以和酸反应,氨气和硫酸反应只能得到硫酸铵 |
某反应的反应过程和能量变化如右图所示,下列有关该反应的叙述正确的是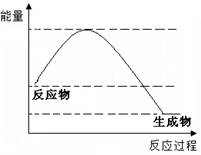
| A.该反应是吸热反应 |
| B.反应物的总能量低于生成物的总能量 |
| C.该反应的反应热△H< 0 |
| D.加入催化剂后反应放出的热会减少 |