用铁片与稀硫酸反应制取氢气时,下列措施可以使氢气生成速率加大的是 ( )
| A.加入少量的硫酸钠 | B.加入硝酸钠固体 |
| C.滴加少量CuSO4溶液 | D.改用浓硫酸 |
下列各溶液中,微粒的物质的量浓度关系正确的是
| A.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B.中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同 |
| C.0. 1 mol·L-1Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| D.a mol·L-1HCN溶液与b mol·L-1NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b |
常温下,pH=10的X、Y两种碱溶液各1 mL,分别稀释至100 mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是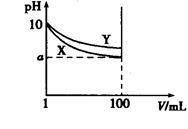
| A.X、Y两种碱溶液中溶质的物质的量浓度一定相等 |
| B.稀释后,X溶液的碱性比Y溶液的碱性强 |
| C.分别完全中和X、Y这两种碱溶液时,消耗同浓度盐酸的体积Vx>Vy |
| D.若8<a<10,则X、Y都是弱碱 |
液氨与水性质相似,也存在微弱的电离:2NH3 NH4++NH2-,其离子积常数K=c(NH4+)·c(NH2-)=2×l0-30,维持温度不变,向液氨中加入少量NH4Cl固体或NaNH2固体,不发生改变的是
NH4++NH2-,其离子积常数K=c(NH4+)·c(NH2-)=2×l0-30,维持温度不变,向液氨中加入少量NH4Cl固体或NaNH2固体,不发生改变的是
| A.液氨的电离度 | B.液氨的离子积常数 |
| C.c(NH4+) | D.c(NH2-) |
用石墨作电极电解100mL H2SO4与CuSO4的混合液,通电一段时间后,两极均收集到2.24 L气体(标准状况),则原混合液中Cu2+ 的物质的量浓度为
| A.1 mol·L-1 | B.2 mol·L-1 | C.3 mol·L-1 | D.4 mol·L-1 |
根据热化学方程式:S(s)+O2(g) 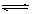 SO2(g);△H =—297.23 kJ. mol—1,分析下列说法正确的是
SO2(g);△H =—297.23 kJ. mol—1,分析下列说法正确的是
A.S(g)+O2(g) SO2(g) ;△H=Q,Q值大于297.23 kJ. mol—1 SO2(g) ;△H=Q,Q值大于297.23 kJ. mol—1 |
B.2S(g)+ 2O2(g) 2SO2(g);△H=—594.46 kJ. mol—1 2SO2(g);△H=—594.46 kJ. mol—1 |
C.SO2(g) S(g)+O2(g);△H=Q,Q值为负值,其绝对值小于297.23 kJ. mol—1 S(g)+O2(g);△H=Q,Q值为负值,其绝对值小于297.23 kJ. mol—1 |
D.SO2(g) S(g)+O2(g) ;△H=Q,Q值为正值,其绝对值大于297.23 kJ. mol—1 S(g)+O2(g) ;△H=Q,Q值为正值,其绝对值大于297.23 kJ. mol—1 |