已知热化学反应方程式:
Zn(s)+ O2(g)
O2(g) ZnO(s);ΔH="-351.5" kJ·mol-1
ZnO(s);ΔH="-351.5" kJ·mol-1
Hg(l)+ O2(g)
O2(g)  HgO(s);ΔH
HgO(s);ΔH  ="-90.84" kJ·mol-1
="-90.84" kJ·mol-1
则锌汞电池中热化学反应方程式:Zn(s)+HgO(s)  ZnO(s)+Hg(l)的ΔH为
ZnO(s)+Hg(l)的ΔH为
| A.ΔH="+260.7" kJ·mol-1 | B.ΔH="-260.7" kJ·mol-1 |
| C.ΔH="-444.2" kJ·mol-1 | D.ΔH="+444.2" kJ·mol-1 |
脑白金主要成分的结构简式为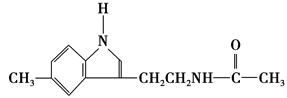
下列对脑白金的推论错误的是( )。
| A.其分子式为C13H16N2O |
| B.能发生水解反应生成乙酸 |
| C.不能与溴水发生反应 |
| D.其官能团及营养成分与葡萄糖相同 |
不久前,欧盟对我国出口的酱油进行检测发现,部分酱油中3氯1,2丙二醇(CH2ClCHOHCH2OH)含量高达10 mg·L-1,超过欧盟规定的该项指标的一千倍。3氯1,2丙二醇和1,3二氯2丙醇统称为“氯丙醇”,都是致癌物。我国就此做了紧急调查并对酱油进行技术处理,使酱油中不含氯丙醇或不超标。技术处理过程中运用的主要反应是( )。
| A.加成反应 | B.氧化反应 | C.消去反应 | D.取代反应 |
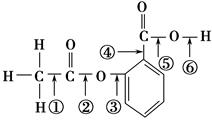
在阿司匹林的结构简式中①②③④⑤⑥分别标出了其分子中的不同的键。将阿司匹林与足量NaOH溶液共煮时,发生反应时断键的位置是( )。
| A.①④ | B.②⑤ | C.③④ | D.②⑥ |
下列说法中,不正确的是( )。
| A.现代药物主要是人工合成的药物 |
| B.天然药物具有良好的药效,所以不需要进行改造 |
| C.药物的生物活性跟它的结构中的某些官能团有关 |
| D.在药物设计领域计算机应用前景广阔 |
天然海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子。火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如下图所示:
下列说法错误的是( )。
| A.天然海水pH≈8的原因是海水中的CO32-、HCO3-水解 |
| B.“氧化”是利用氧气将H2SO3、HSO3-、SO32-等氧化生成SO42- |
| C.“反应、稀释”时加天然海水的目的是中和、稀释经氧气氧化后海水中生成的酸 |
| D.“排放”出来的海水中SO42-的物质的量浓度与进入吸收塔的天然海水相同 |