(1 0分)汽车尾气中含有CO、NO2
0分)汽车尾气中含有CO、NO2 等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化成无毒气体。
等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化成无毒气体。
(1)汽油在不同空/燃比(空气与燃油气的体积比)时尾气的主要成分不同,空/燃比较小时的有毒气体主要是 ▲ (填化学式)。
(2)人们把拆开1 mol化学键所吸收的能量看成该化学键的键能。
已知:N2、O2分子中化学键的键能分别是946 kJ·mol-1、497 kJ·mol-1。
查阅资料获知如下反应的热化学方程式:
N2(g)+O2(g)=2NO(g) ΔH=+180 kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+68 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
C(s)+O2(g)=CO2 (g) ΔH=-393.5 kJ·mol-1
(g) ΔH=-393.5 kJ·mol-1
① 一定条件下,N2与O2反应生成NO能够自发进行,其原因是 ▲ ;NO分子中化学键的键能为 ▲ kJ·mol—1。
② CO与NO2反应的热化学方程式为4CO(g)+2NO2(g)=4CO2(g)+N2(g) ΔH= ▲ 。对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是 ▲
ΔH= ▲ 。对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是 ▲  (填代号)。
(填代号)。
(9分)下表为元素周期表的一部分,请回答有关问题:
| IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
| 2 |
① |
② |
||||||
| 3 |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
||
| 4 |
⑨ |
⑩ |
(1)表中最活泼的金属是______,非金属性最强的元素是______;(填写元素符号)
(2) 最高价氧化物对应水化物酸性最强的化合物是__________;(填写分子化学式)
(3)表中能形成两性氢氧化物的元素是_______,分别写出该元素的氢氧化物与⑥、⑨的最高价氧化物对应水化物反应的离子反应方程式:
_____________________,___________________________;
(4)比较⑦、⑩单质氧化性的强弱:__________________________。
有A、B、C、D四种短周期元素, 它们的原子序数由A到D依次增大,已知A和B 原子有相同的电子层数, 且A的L层电子数是K层电子数的两倍, C在空气中燃烧时呈现黄色火焰, C的单质在高温下与B的单质充分反应, 可以得到与D单质颜色相同的淡黄色固态化合物, 试根据以上叙述回答:
(1)元素名称: A ______ B _____ C _____ D ______。
(2)D元素位于周期表中周期族。
(3)写出AB2与C2B2反应的化学方程式。
(4)画出B的原子结构简图 ___________________。
(5)电子式表示化合物 C2D:。
用“大于”或“小于”或“等于”回答下列问题:
(1)酸性:H2CO3H2SiO3, H2SiO3H3PO4
(2)碱性:Ca(OH)2Mg(OH)2, Mg(OH)2Al(OH)3
(3)气态氢化物稳定性:H2OH2S, H2SHCl
(4)还原性: H2OH2S, H2SHCl
(5)酸性: H2SO4H2SO3, HClO4HClO
从以上答案中可以归纳出:
①元素的非金属性越强,其对应最高价氧化物水化物的酸性越;
②元素的金属性越强,其对应最高价氧化物水化物的碱性越。
、4g甲烷在氧气中燃烧生成二氧化碳和液态水,放出222.5KJ热量,写出甲烷燃烧的热化学方程式
有下列各组微粒或物质:
A、O2和O3B、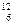 C和
C和 C C、CH3CH2CH2CH3和
C C、CH3CH2CH2CH3和
(1)组两种微粒互为同位素;
(2)组两种物质互为同素异形体;
(3)组两物质互为同分异构体;
(4)组两物质是同一物质。