1 g碳与适量水蒸气反应生成CO和H2,需吸收10.94 kJ热量,此反应的热化学方程式为
| A.C+H2O=CO+H2;△H="+131.3" kJ·mol-1 |
B.C(s)+H2O(g)=CO(g)+H2( g);△H="+10.94" kJ·mol-1 g);△H="+10.94" kJ·mol-1 |
| C.C(s)+H2O(l)=CO(g)+H2(g);△H="+131.3" kJ·mol-1 |
| D.C(s)+H2O(g)=CO(g)+H2(g);△H="+131.3" kJ·mol-1 |
同温同压下,等质量的下列气体所占有的体积最大的是
| A.O2 | B.CH4 | C.CO2 | D.SO2 |
设NA为阿伏加德罗常数,下列说法正确的是:
| A.标准状况下,5.6L四氯化碳含有的分子数为0.25NA |
| B.标准状况下,22.4LCH4中含有的分子总数为5NA |
| C.常温常压下,14g氮气含有的原子数为NA |
| D.标准状况下,铝跟盐酸溶液反应生成1mol氢气时,转移的电子数为NA |
下列说法正确的是
| A.硫酸、纯碱、硝酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B.根据元素种类的多少将物质分为纯净物和混合物 |
| C.通常情况下,若发生反应A2 + 2B-= 2A-+ B2,则氧化剂是A2 |
| D.碳酸氢钠在水中的电离方程式:NaHCO3=Na++H++CO32- |
下列反应的离子方程式正确的是
| A.金属镁与稀盐酸反应 :Mg+2H++2Cl-===MgCl2+H2↑ |
B.氯化钡溶液与硫酸反应 :Ba2++ SO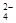 ===BaSO4↓ ===BaSO4↓ |
| C.碳酸钠溶液与盐酸反应 :Na2CO3+2H+===2Na++H2O+CO2↑ |
| D.氢氧化镁与硫酸溶液反应:OH-+H+===H2O |
影响一定数量气体体积大小的主要因素是
| A.气体分子的摩尔质量 | B.微粒本身的大小 |
| C.微粒的质量 | D.微粒间的平均距离 |