下列说法正确的是(设阿伏加德罗常数的数值为6.02×1023)( )。
| A.在标准状况下,22.4 L苯所含分子数目为6.02×1023 |
| B.1 mol/L K2SO4溶液所含K+数目为2×6.02×1023 |
| C.在常温常压下,16 g 02和03的混合气体所含原子数目为6.02×1023 |
| D.2.4 g Mg与足量盐酸完全反应时,失去电子数目为O.1x 6.02×1023 |
下列实验装置,试剂选用或操作正确的是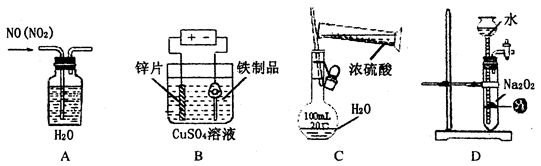
| A.除去NO中的NO2 | B.铁制品表面镀锌 |
C.稀释浓硫酸 |
D.制备少量O2 |
在允许加热的条件下,只用一 种试剂就可以鉴别(NH4)2SO4、KCl、MgCl2、Al2(SO4)3和Fe2(SO4)3溶液,这种试剂是
种试剂就可以鉴别(NH4)2SO4、KCl、MgCl2、Al2(SO4)3和Fe2(SO4)3溶液,这种试剂是
| A.NaOH | B.NH3·H2O | C.AgNO3 | D.BaCl2 |
在同一溶液中,含有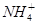 、I-、Ba2+、Cl-等离子,则该溶液的pH和介质是
、I-、Ba2+、Cl-等离子,则该溶液的pH和介质是
| A.pH=1,硝酸溶液为介质 | B.pH=3,硫酸溶液为介质 |
| C.pH=8,次氯酸钠溶液为介质 | D.pH=12,氨水为介质 |
下列用来表示物质变化的化学反应中,正确的是
A.钢铁腐蚀时可能发生的正极反应:4OH--4e- 2H2O+O2↑ 2H2O+O2↑ |
B.表示中和热的离子方程式:H++OH- H2O;△H=-57.3kJ/mol H2O;△H=-57.3kJ/mol |
C.明矾水解反应的离子方程式:Al3++3H2O Al(OH)3+3H+ Al(OH)3+3H+ |
D.硫酸铵溶液与氢氧化钠溶液混合共热的离子方程式: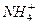 +OH- +OH-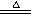 NH3↑+H2O NH3↑+H2O |
有①Na2CO3溶液、②CH3COONa溶液、③NaOH溶液各25mL,物质的量浓度均为0.1mol/L,下列说法正确的是
| A.三种溶液pH的大小顺序是③>②>① |
| B.若将三种溶液稀释相同倍数,pH变化最大的是② |
| C.若分别加入25mL 0.1mol/L盐酸后,pH最大的是① |
| D.若三种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>② |