氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300-1700oC的氮气流中反应制得3SiO2(s)+6C(s)+2N2(g)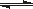 Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)
(1)已知该反应每转移1mole—,放出132.6kJ的热量,该方程式的?H = 。
(2)能判断该反应(在体积不变的密闭容器中进行)已经达到平衡状态的是 。
A.焦炭的质量不再变化 B.N2和CO速率之比为1:3
C.生成6molCO同时消耗1mol Si3N4 D.混合气体的密度不再变化
(3)下列措施中可以促进平衡右移的是 。
A.升高温度 B.降低压
C.加入更多的SiO2 D.充入N2
某温度下,测得该反应中N2和CO各个时刻的浓度如下,
| 时间/min |
0 |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
40 |
45 |
| N2浓度/mol·L-1[ |
4.00 |
3.70 |
3.50 |
3.36 |
3.26 |
3.18 |
3.10 |
3.00 |
3.00 |
3.00 |
| CO浓度/mol·L-1 |
0.00 |
0.90 |
1.50 |
1.92 |
2.22 |
2.46 |
2.70 |
— |
— |
— |
求0—20 min内N2的平均反应速率V(N2 )= ,该温度下,反应的平衡常数K= 。
⑴某化学兴趣小组对“农夫山泉”矿泉水进行检测时,发现1.0 L该矿泉水中含有45.6 mg Mg2+的物质的量浓度为____________。
⑵在KCl和CaCl2所组成的某混合物中,KCl与CaCl2的物质的量之比为2:1,则K+与Ca2+的物质的量之比为____________,该混合物中的CaCl2的质量分数为____________ 。
计算: (1) 2mol NH3中含有____________________个NH3分子, ___________________个N原子,___________________个H原子;
(2)1mol CaCl2中含 ____mol Ca2+,______mol Cl-,共________mol离子
(3)H2SO4的摩尔质量是_________ _,9.8g H2SO4的物质的量是______mol, ______g的硫元素,______g的SO42-。
_,9.8g H2SO4的物质的量是______mol, ______g的硫元素,______g的SO42-。
(4)标准状况下有(1)6.72L CH4 (2) 3.01×1023个HCl分子(3)13.6g H2S,下列对这三种气体的关系从小到大的排列顺序是:
| A.物质的量______________ | B.体积___________________ |
| C.质量__________________ | D.氢原子数_______________ |
(14分)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
(1)目前工业上有一种方法是用CO2来生产燃料甲醇。
为探究反应原理,现进行如下实验,在体积为1 L的 密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g)
密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol
CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol
测得CO2和CH3OH(g)的浓度随时间变化如图所示。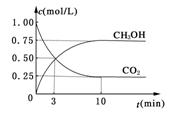
①从反应开始到平衡,氢气的平均反应速率υ(H2)=__________mol/(L·mi n)。
n)。
②该反应的平衡常数表达式为K=__________。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1277 kJ·mol-1
ΔH=-1277 kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1
③C(s)+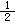 O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
④H2O(g)=H2O(l) ΔH=-44 kJ·mol-1
则,CH3OH(l)+O2(g)=CO(g)+2H2O(l) ΔH=________kJ·mol-1。
(3)2009年10月 ,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。
,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。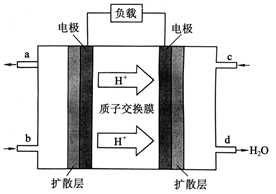
①该电池工作时,b口通入的物质为___________,c口通入的物质为___________。
②该电池负极的电极反应式为:_________________。
③工作一段时间后,当外电路中有1.2NA个电子通过时,有 g甲醇参加反应。
(4)在下列选项中与甲醇互为同系物的是_______(填字母代号),该同系物与相对分子质量相同的羧酸反应的化学方程式为______________,该反应的反应类型是____________。
试写出一种与D选项互为同分异构体且含有苯环的物质_______________。
(11分)氨在工农业生产中应用广泛。在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如下:
| 温度/℃ |
200 |
300 |
400 |
500 |
600 |
| 氨含量/% |
89.9 |
71.0 |
47.0 |
26.4 |
13. 8 8 |
请回答:
(1)根据表中数据,结合化学平衡移动原理,说明合成氨反应是放热反应的原因是_____________________________________________________________________________。
(2)根据表中数据,在500℃合成氨反应达到平衡时,与反应前的体积相比,反应后体积缩小的百分率是____________(保留2位有效数字)。
(3)在一定温度下,将2 mol N2和6 mol H2通入到体积为2 L的密闭容器中,发生反应
N2+3H2 2NH3,2 min达到平衡状态时,H2转化率是50%,该温度下的平衡常数K=______________(用分数表示);欲使K增大,可以采取的措施是___________________。
2NH3,2 min达到平衡状态时,H2转化率是50%,该温度下的平衡常数K=______________(用分数表示);欲使K增大,可以采取的措施是___________________。
(4)从化学平衡移动的角度分析,提高H2转化率可以采取的措施是______(选填序号字母)
a.及时分离出NH3 b.升高温度c.增大压强 d.使用催化剂
(5)NH3也能分解为N2和H2,在相同条件下,测得分解后混合气体密度为分解前的2/3,则氨的分解率为_______。
(6)根据下图的能量变化,求下列反应的反应热。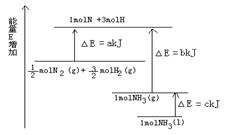
N2(g)+3H2(g) 2NH3(l)△H=___________。
2NH3(l)△H=___________。
(10分)将乙醇和汽油按一定比例混配作为燃料,可缓解能源供应紧张的矛盾。请回 答下列问题:
答下列问题:
(1)写出由“纤维素→葡萄糖→乙醇”中的由“纤维素→葡萄糖”的化学方程式:
_______________________________________。
(2)已知 4.6g 乙醇完全燃烧生成 CO2 和液态水放出热量 136kJ ,请写出乙醇燃烧的热化学方程式_______________________________________。
(3)血液中含乙醇 0.1 %会使视觉敏感度降到 32 % ,因此交通法规定严禁酒后驾车。一种简便的检测方法是让驾车人呼出的气体接触含有经硫酸酸化处理的强氧化剂(CrO3)的硅胶,如果呼出的气体中含乙醇蒸汽,乙醇会被氧化生成乙醛,同时 CrO3被还原为硫酸铬 [Cr2(SO4)3],请写出检测时反应的化学方程式____________________________________。
(4)为了验证乙醇的氧化反应,同学们设计了如下两种装置: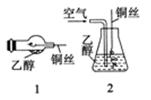
①装置1是在容器内加入乙醇后稍加热,操作铜丝的方法是___________________________,会发现铜丝由黑变红,写出反应的化学方程式:___________________________________。
②某同学按照装置2所示进行操作,当给锥形瓶加 热一段时间后,并没有闻到乙醛的刺激性气味,其原因是_______________________________________________________。
热一段时间后,并没有闻到乙醛的刺激性气味,其原因是_______________________________________________________。