已知反应: 某温度下,将2molSO2和1mol O2置于10L密闭容器中,反应达平衡后,SO2的平衡转化率(a)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
某温度下,将2molSO2和1mol O2置于10L密闭容器中,反应达平衡后,SO2的平衡转化率(a)与体系总压强(p)的关系如图甲所示。则下列说法正确的是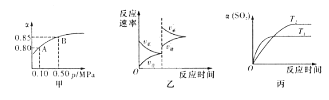
| A.由图甲知,A点SO2的平衡浓度为0.4mol/L |
| B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2:1:2 |
| C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示 |
| D.压强为0.50MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1 |
温室效应产生的原因之一是大气中CO2的含量剧增,要想减缓这一现象的发生,最理想的燃料是
| A.天然气 | B.氢气 | C.液化石油气 | D.酒精 |
在2A+B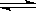 3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是
A.υ(A)= 0.5 mol/(L·s) B.υ(B)= 0.3 mol/(L·s)
C.υ(C)= 0.8 mol/(L·s) D.υ(D)= 1 mol/(L·s)
分别放置在如下图所示装置(都盛有0.1 mol·L-1的H2SO4溶液)中的四个相同的纯锌片,腐蚀最快的是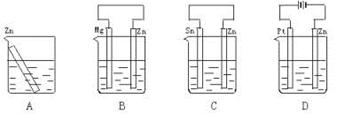
一定温度下,向aL密闭容器中加入2molNO2(g),发生如下反应:2NO2 2NO + O2,此反应达到平衡状态时的标志是
2NO + O2,此反应达到平衡状态时的标志是
| A.混合气体的颜色变浅 |
| B.混合气体的物质的量相等 |
| C.混合气中NO2、NO、O2物质的量之比为2:2:1 |
| D.单位时间内生成2nmolNO同时生成2nmolNO2 |
下列说法正确的是
| A.电能是二级能源 | B.天然气是二级能源 |
| C.水煤气是一级能源 | D.风力是二级能源 |