有关AgCl沉淀的溶解平衡说法正确的是( )
| A.AgCl沉淀生成和沉淀溶解不断进行并且速率相等 |
| B.AgCl难溶于水,溶液中没有Ag+和Cl- |
| C.升高温度,AgCl沉淀的溶解度减小 |
| D.向AgCl沉淀中加入NaCl固体,AgCl沉淀的溶解平衡不移动 |
已知次氯酸是比碳酸还弱的酸,反应Cl2 + H2O HCl + HClO达平衡后,要使HClO浓度增大,可加入
HCl + HClO达平衡后,要使HClO浓度增大,可加入
| A.足量6mol/L NaOH溶液 | B.少量6mol/L H2SO4溶液 |
| C.少量NaHCO3固体 | D.足量Na2SO3溶液 |
在相同温度时,100mL 0.01mol·L-1的醋酸溶液与10mL 0.1mol·L-1的醋酸溶液相比较,下列数值中,前者大于后者的是
| A.H+的物质的量 | B.醋酸的电离常数 |
| C.中和时所需NaOH的量 | D.CH3COOH的物质的量 |
由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH=1,c(Al3+)=0.4mol·L-1,c(SO42-)=0.8mol·L-1,则c(K+)为
| A.0.15 mol·L-1 | B.0.2 mol·L-1 |
| C.0.3 mol·L-1 | D.0.4 mol·L-1 |
下图曲线a表示放热反应X(g)+Y(g) Z(g)+M(g)+ N(s) 进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
Z(g)+M(g)+ N(s) 进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是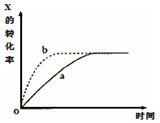
| A.减小体积 | B.加大X的投入量 |
| C.减压 | D.升高温度 |
下列措施或事实不能用勒夏特列原理解释的是
| A.新制的氯水在光照下颜色变浅 |
| B.H2、I2、HI平衡混合气加压后颜色变深 |
| C.在合成氨的反应中,降温或加压有利于氨的合成 |
| D.Fe(SCN)3溶液中加入6mol/L NaOH溶液后颜色变浅 |