某小组为研究电化学原理,设计如图2装置。下列叙述不正确的是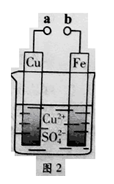
| A.a和b不连接时,铁片上会有金属铜析出 |
| B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu |
| C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
| D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动 |
下列化学(或离子)方程式正确的是
A.乙酸与碳酸钠溶液反应:2H++CO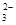 =CO2↑+H2O =CO2↑+H2O |
B.C6H6+HNO3 C6H5NO2+H2O C6H5NO2+H2O |
C.亚硫酸的电离方程式:H2SO3 2H++SO32- 2H++SO32- |
| D.醋酸溶液与新制氢氧化铜反应:CH3COOH+OH-→ CH3COO-+H2O |
有两种气态烃组成的混合气完全燃烧后所得到的CO2和H2O的物质的量随混合烃的总物质的量的变化如下图所示,则下列对混合烃的判断正确的是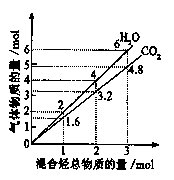
①一定有乙烯;②一定有甲烷;③一定有丙烷;④一定无乙烷;⑤可能有乙烷
| A.①②⑤ | B.②④ | C.②⑤ | D.②③ |
现有三组混合液:(1)乙酸乙酯和乙酸钠水溶液;(2)乙醇和丁醇;(3)溴化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
| A.分液、萃取、蒸馏 | B.萃取、分液、蒸馏 |
| C.萃取、蒸馏、分液 | D.分液、蒸馏、萃取 |
工业上或实验室提纯以下物质的方法不合理的是(括号内为杂质)
| A.硝基苯(二氧化氮):加NaOH溶液,分液 |
| B.乙烷(乙烯):催化加氢 |
| C.乙醇(水):加新制生石灰,蒸馏 |
| D.油脂皂化反应产物中分离出高级脂肪酸钠:加NaCl,过滤 |
日常生活中遇到的很多问题都涉及到化学知识,下列有关做法在日常生活中可行的是
| A.医用酒精和工业酒精的主要成分相同,都可用于伤口消毒 |
| B.可利用米汤检验含碘盐的真假 |
| C.低血糖症状出现时,吃馒头要比喝葡萄糖水见效快 |
| D.人体对食物中蛋白质的消化其实就是使蛋白质发生了水解 |