(NH4)2PtCl6晶体受热分解,生成氮气、氯化氢、氯化铵和金属铂。在此分解反应中,氧化产物与还原产物的物质的量之比是
| A.2∶3 | B.3∶2 | C.4∶3 | D.1∶3 |
100 mL 6mol/L H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的
| A.碳酸钠(s) | B.醋酸钠(s) | C.硫化钠(溶液) | D.硫酸钾(s) |
在容积一定的密闭容器中发生可逆反应A(g)+2B(g)  2C(g)-Q,平衡移动关系如图所示。下列说法正确的是
2C(g)-Q,平衡移动关系如图所示。下列说法正确的是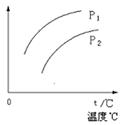
| A.P1>P2,纵坐标指A的质量分数 |
| B.P1> P2,纵坐标指C的质量分数 |
| C.P1< P2,纵坐标指A的转化率 |
| D.P1< P2,纵坐标指混合气体的平均摩尔质量 |
工业制硫酸铜不是直接用铜和浓硫酸反应,而是将粗铜(含少量银)浸入稀硫酸中,并不断从容器下部吹入细小的空气泡。有关该制备方法的叙述中,正确的是
①该方法应用了原电池工作原理②该方法应用了电解池工作原理
③该方法不产生污染大气的二氧化硫④该方法提高了硫酸的利用率
⑤该方法提高了铜的利用率
| A.①③⑤ | B.②③ | C.①③④ | D.①③④⑤ |
可用右图装置制取(必要时可加热)、净化、收集的气体是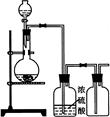
| A.铜和稀硝酸制一氧化氮 | B.氯化钠与浓硫酸制氯化氢 |
| C.锌和稀硫酸制氢气 | D.硫化亚铁与稀硫酸制硫化氢 |
已知某溶液中存在较多的H+、SO42-、NO3-,则溶液中还可能大量存在的离子组是
| A.A13+、CH3COO—、C1— | B.Na+、NH4+、C1— |
| C.Mg2+、C1—、Fe2+ | D.Mg2+、Ba2+、Br— |