某二元酸(H2A)按下式发生电离:H2A=H++HA-;HA-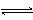 H++A2-。现有下列四种溶液①0.0lmol/L的H2A溶液②0.0lmol/L的NaHA溶液 ③0.02mol/L的HC1溶液与0.04mol/L的NaHA溶液等体积混合④0.02mol/L的NaOH溶液与0.02mol/L的NaHA溶液等体积混合
H++A2-。现有下列四种溶液①0.0lmol/L的H2A溶液②0.0lmol/L的NaHA溶液 ③0.02mol/L的HC1溶液与0.04mol/L的NaHA溶液等体积混合④0.02mol/L的NaOH溶液与0.02mol/L的NaHA溶液等体积混合
下列关于上述四种溶液的说法正确的是 ( )
A.溶液②中存在水解平衡:HA-+H2O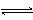 H2A+OH-
H2A+OH-
B.溶液③中有:c(HA-)+c(A2一)=c(Na+)
C.溶液④中有:c(OH一)=c(H+) +c(HA-) +2c(H2A)
D.四种溶液中c(HA-)浓度大小:③>②>①>④
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
N2(g) + 3H2(g)  2NH3(g)△H=-92.4 kJ/mol。
2NH3(g)△H=-92.4 kJ/mol。
实验测得起始.平衡时的有关数据如下表:
| 容器编号 |
起始时各物质物质的量/mol |
平衡时反应中的能量变化 |
||
| N2 |
H2 |
NH3 |
||
| ① |
1 |
3 |
0 |
放出热量a kJ |
| ② |
2 |
3 |
0 |
放出热量b kJ |
| ③ |
2 |
6 |
0 |
放出热量c kJ |
下列叙述正确的是
A.放出热量关系:a < b < 92.4
B.三个容器内反应的平衡常数:③> ①> ②
C.平衡时氨气的体积分数:①> ③
D.N2的转化率:②> ①> ③
反应aM(g)+bN(g)  cP(g)+dQ(g)达到平衡时,M的体积分数y(M)与反应条件的关系如图所示。其中z表示反应开始时N的物质的量与M的物质的量之比。下列说法正确的是( )
cP(g)+dQ(g)达到平衡时,M的体积分数y(M)与反应条件的关系如图所示。其中z表示反应开始时N的物质的量与M的物质的量之比。下列说法正确的是( ) 
| A.同温同压同z时,加入催化剂,平衡时Q的体积分数增加 |
| B.同压同z时,升高温度,平衡时Q的体积分数增加 |
| C.同温同z时,增加压强,平衡时Q的体积分数增加 |
| D.同温同压时,增加z,平衡时Q的体积分数增加 |
化学平衡状态I、II、III的相关数据如下表:
| 编号 |
化学方程式 |
平衡常数 |
温度 |
|
| 979K |
1173K |
|||
| I |
Fe(s)+CO2(g)  FeO(s)+CO(g) FeO(s)+CO(g) |
K1 |
1.47 |
2.15 |
| Ⅱ |
CO(g)+H2O(g)  CO2(g)+H2(g) CO2(g)+H2(g) |
K2 |
1.62 |
b |
| Ⅲ |
Fe(s)+H2O(g)  FeO(s)+H2(g) FeO(s)+H2(g) |
K3 |
a |
1.68 |
根据以上信息判断,下列结论错误的是
A.a>b
B.增大压强,平衡状态II不移动
C.升高温度平衡状态III向正反应方向移动
D.反应II、III均为放热反应
某温度下在容积不变的密闭容器中发生如下反应:2SO2+O2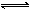 2SO3(g),若开始时只充入2 molSO3(g),达到平衡时,混合气体的压强比起始时增大了20%;若开始时只充入了2 mol SO2和1 molO2的混合气体,达到平衡时SO2的转化率为
2SO3(g),若开始时只充入2 molSO3(g),达到平衡时,混合气体的压强比起始时增大了20%;若开始时只充入了2 mol SO2和1 molO2的混合气体,达到平衡时SO2的转化率为
| A.20% | B.40% | C.50% | D.60% |
在容积不变的密闭容器中,在一定条件下发生反应:2A(?) B (g)+C(s),且达到平衡,当升高温度时,容器内气体的密度变大,则下列判断错误的是
B (g)+C(s),且达到平衡,当升高温度时,容器内气体的密度变大,则下列判断错误的是
| A.若正反应为吸热反应,则A为非气态 |
| B.若正反应为放热反应,则A为气态 |
| C.若在平衡体系中加入少量C,则该平衡不移动 |
| D.压强对该平衡的移动无影响 |