将mg含氧化铁、氧化铜和氧化亚铁的样品投入物质的量浓度为1mol/L的2L盐酸溶液中恰好完全反应,若向等质量的该样品通入足量的氢气并加热充分反应后所得金属的质量是
| A.(m-16)g | B.(m+16)g | C.(m-32)g | D.16g |
可逆反应mA(g)+nB(g) pC(g)+gD(g)的v-t图象如下图甲,若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图象如下图乙。()
pC(g)+gD(g)的v-t图象如下图甲,若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图象如下图乙。()
①a1=a2②a1<a2③b1=b2④b1<b2⑤t1>t2⑥t1=t2
⑦两图中阴影部分面积相等⑧乙图阴影部分面积更大,以上正确的为( )
| A.①③⑥⑦ | B.①④⑥⑧ | C.②③⑤⑧ | D.②④⑤⑦ |
有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法不正确的是 ()
①在标准状况下,每消耗5.6L CH4可以向外电路提供2mole-
②通过甲烷电极的电极反应式为:CH4+10OH--8e-=CO32-+7H2O
③通过甲烷的电极为电池的正极,通过氧气的电极为负极
④电池放电后,溶液PH不断升高
| A.①② | B.①③ | C.①④ | D.③④ |
某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2===2H2O,下列有关说法正确的是 ( )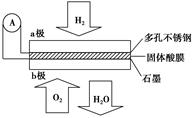
| A.电子通过外电路从b极流向a极 |
| B.b极上的电极反应式为:O2+2H2O+4e-―→4OH- |
| C.每转移0.1 mol电子,消耗1.12 L的H2 |
| D.H+由a极通过固体酸电解质传递到b极 |
下列说法正确的是()
| A.分子晶体中一定存在分子间作用力,不一定存在共价键 |
| B.含有极性键的分子一定是极性分子 |
| C.含有金属离子的晶体一定是离子晶体 |
| D.元素的非金属型越强,其单质的活泼型一定越强 |
分子式为C5H11Cl的同分异构体共有(不考虑立体异构)
| A.6种 | B.7种 | C.8种 | D.9种 |