某无色溶液中可能含有Na+、Fe2+、Br-、 CO32-、I-、SO32-六种离子中的几种。①在该溶液中滴加足量氯水后,有气泡产生、溶液呈橙黄色;②向呈橙黄色的溶液中加入BaCl2溶液时无沉淀生成;③向淀粉溶液中滴加橙黄色溶液未变蓝色。根据上述实验事实推断,在该溶液中肯定存
CO32-、I-、SO32-六种离子中的几种。①在该溶液中滴加足量氯水后,有气泡产生、溶液呈橙黄色;②向呈橙黄色的溶液中加入BaCl2溶液时无沉淀生成;③向淀粉溶液中滴加橙黄色溶液未变蓝色。根据上述实验事实推断,在该溶液中肯定存 在的离子组是( )。
在的离子组是( )。
A.Na+、Br-、CO32- B.Na+、 I-、SO32-
C .Fe2+、I-、SO32- D.Fe2+、Br-、CO32-
.Fe2+、I-、SO32- D.Fe2+、Br-、CO32-
将17.9gAl、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生气体3.36L(标准状况)。另取等质量的合金溶于过量的稀硝酸中,生成6.72L NO(标准状况,唯一还原产物),向反应后的溶液中加入过量的NaOH溶液,得到沉淀的质量为( )
)
| A.33.2g | B.25.4g | C.22.4g | D.19.6g |
将0.4gNaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是()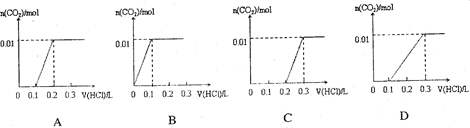
一定量的铁与一定量的浓HNO3反应,得到硝酸铁溶液和NO2、N2O4、NO的混合气体,这些气体与3.36 L O2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成硝酸。若向所得硝酸铁溶液中加入2 mol·L-1的NaOH 溶液至Fe3+恰好沉淀,则消耗NaOH溶液的体积是( )
| A.300mL | B.150mL | C.120mL | D.90mL |
查处酒后驾驶采用的“便携式乙醇测量仪”以燃料电池为工作原理,在酸性环境中,理论上乙醇可以被完全氧化为CO2,但实际乙醇被氧化为X,其中一个电极的反应式为:
CH3CH2OH-2e-→X+2H+。下列说法中正确的是( )
A.电池内部H+由正 极向负极移动 极向负极移动 |
| B.另一极的电极反应式为:O2 + 4e- + 2H2O = 4OH- |
| C.乙醇在正极发生反应,电子经过外电路流向负极 |
| D.电池总反应为:2CH3CH2OH+O2→2CH3CHO+2H2O |
某同学在实验室进行了如图所示的实验,下列说法中错误的是()
| A.利用过滤的方法,可将Z中固体与液体分离 |
| B.X、Z烧杯中分散质相同 |
| C.Y中反应的离子方程式为:3CaCO3+2Fe3++3H2O====2Fe(OH)3+3CO2↑+3Ca2+ |
| D.Z中分散系能产生丁达尔效应 |