海洋是丰富的化学资源宝库。通过晾晒海水,可以得到含少量泥沙的粗盐。未来得到纯净的NaCl(不考虑可溶性杂质),设计了如图所示的实验操作:
(1)上图有标号的仪器名称分别是a ,b 。
(2)操作②的名称是 ,玻璃棒的作用是 。
(3)操作③中看到 时,停止加热。
(4)称取5.0gNaCl固体,可配制溶质质量分数为10%NaCl溶液 g。
(15分)请根据要求填空:
(1)用化学用语填写下列空白:
①2个氢原子;②3个氧分子;③氯离子;
④水;⑤氧化铝中铝元素的化合价为价。
(2)写出下列反应的化学方程式:
①硫在氧气中燃烧;
②一氧化碳在高温条件下还原三氧化二铁。
(3)我们学习过的一些物质,在实际生活中有着重要的用途。现有下列物质:
| A.乙醇 | B.活性炭 | C.稀有气体 | D.镁 E、二氧化碳 F、氧气。请根据它们的用途,用字母代号填空: |
①可供给呼吸,急救病人;②可用于制干冰、温室气体肥料;
③可用高梁、玉米和薯类等经过发酵而制得,该物质可做酒精灯燃料;
④可用作冰箱的除臭剂;⑤可在通电时能发出不同颜色的光;
⑥可用于制作造明弹,它在空气中燃烧发出耀眼的白光。
某同学用右图所示装置进行验证燃烧条件的实验。取一小块白磷放入广口瓶中,一段时间白磷没有燃烧,然后从分液漏斗中加入适量的热水,白磷仍然没有燃烧,再从a管通入,白磷发生燃烧,该实验(填“能”或“不能”)证明可燃物燃烧需要与氧气接触、温度达到着火点这两个条件。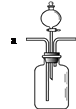
某同学配制100克6%的NaCl溶液,需要NaClg,其中钠元素的质量是
g(保留小数点后两位数字)。应选择mL量筒量取水,该同学量取水时仰视读数,则配制溶液的质量分数将(填“>”或“<”或“=”)6%;若该同学在称量氯化钠时发现天平指针向右偏转,则他应该进行的操作是。
形态各异的物质可按一定规律分类。现有A硫酸钠B液氧C空气D氯化钠
E冰水混合物F水银 六种物质,请选用合适的物质填空。
(1)属于混合物的是(填序号);
(2)含有氧分子的是(填序号);
(3)属于由离子构成的不含原子团的化合物是(填化学式);
(4)属于氧化物的是(填化学式)。
用化学用语填空:
(1)保持二氧化碳化学性质的最小粒子是:;
(2)地壳中含量最高的金属元素和非金属元素组成的化合物:;
(3)正三价的铁的氧化物:;
(4)氧化镁中镁元素显正二价:;
(5)天然气的主要成分:;
(6)2个硫酸根离子:。