下列实验操作中,错误的是
| A.制取蒸馏水时,为防止烧瓶内产生暴沸现象,应事先向烧瓶中加入几片碎瓷片 |
| B.测定未知NaOH溶液浓度时,酸式滴定管需用标准酸液润洗2—3次 |
| C.配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释 |
| D.燃着的酒精灯不慎碰翻失火,应立即用湿布盖灭 |
下图为分离乙酸乙酯、乙酸和乙醇混合物的实验操作流程图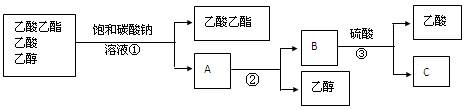
在上述实验过程中,所涉及的三次分离操作分别是
| A.①蒸馏 ②过滤 ③分液 | B.①分液 ②蒸馏 ③蒸馏 |
| C.①蒸馏 ②分液 ③分液 | D.①分液 ②蒸馏 ③过滤 |
“塑料王”又称聚四氟乙烯,其链节是
A.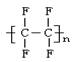 |
B.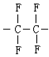 |
C.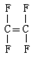 |
D.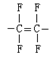 |
分子式C4H8O2的有机物与硫酸溶液共热可得有机物A和B。将A氧化最终可得C,且B和C为同系物。若B可发生斐林反应,则原有机物的结构简式为
A.HCOOCH2CH2CH3 B.CH3COOCH2CH3
C.CH3CH2COOCH3 D.HOCH2CH2CH2CHO
在3H2(g)+N2(g) 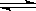 2NH3(g)的反应中,经过一段时间后,NH3的浓度增加了0.6mol·L-1,此时间内用H2表示的平均速率为0.45mol·L-1·s-1,则这段时间是
2NH3(g)的反应中,经过一段时间后,NH3的浓度增加了0.6mol·L-1,此时间内用H2表示的平均速率为0.45mol·L-1·s-1,则这段时间是
| A.1s | B.0.44s | C.1.33s | D.2s |
镁铝合金在碱性溶液中开始反应缓慢,后反应加速。经分析是氧化膜及微小原电池作用的结果。下列叙述正确的是
| A.原电池的负极是镁 | B.负极的电极反应式是Mg-2e = Mg2+ |
| C.原电池的负极是铝 | D.正极的电极反应式是2H++2e = H2↑ |