室温下,将1.000 mo1/L盐酸滴入20.00mL l.000 mol/L
氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所
示。下列有关说法正确的是( )
| A.a点由水电离出的c(H+)=1.0×l0-14mol/L |
| B.b点:c(NH4+)+c(NH3·H2O)=c(CI—) |
| C.c点:c(Cl—)= c(NH4+) |
| D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热 |
下列离子方程式错误的是
| A.钾和水反应:2K + 2H2O = 2K+ + 2OH- +H2↑ |
| B.氯化铝溶液加入过量氨水:Al3+ + 3OH- = Al(OH)3 ↓ |
| C.将Cl2通入氯化亚铁溶液: 2Fe2+ + Cl2 = 2Fe3+ + 2Cl- |
| D.氢氧化钡溶液和硫酸铜溶液反应: |
Ba2+ + 2OHˉ + Cu2+ + SO42ˉ= BaSO4↓ + Cu(OH)2↓
用氯气消毒过的自来水配制下列溶液时,会使配得的溶液变质的是
①NaOH②AgNO3③Na2CO3④FeCl2
| A.②④ | B.①②③ | C.①③ | D.①②③④ |
下列反应制取气体合理可行的是
| A.Zn + 2HNO3(稀)= Zn(NO3)2 + H2↑ |
B.CaCO3 + H2SO4(稀)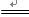 CaSO4 + H2O + CO2↑ CaSO4 + H2O + CO2↑ |
C.NH4Cl(aq) + NaOH(aq)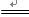 NaCl + H2O + NH3↑ NaCl + H2O + NH3↑ |
D.MnO2 + 4HCl(浓) 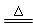 MnCl2 + Cl2↑+ 2H2O MnCl2 + Cl2↑+ 2H2O |
德国人弗里茨•哈伯(Fritz Haber)由于发明了合成氨的方法而获得了1918年诺贝
尔化学奖,他的发明大大提高了农作物的产量,同时也提高了硝酸、炸药的产量。下列有关说法正确的是
| A.N2和H2在点燃或光照条件下合成氨 |
| B.氨的稳定性比磷化氢弱 |
| C.氨极易溶于水,氨水呈碱性,主要含 NH4+和OH- |
| D.由氨制取硝酸铵的过程中,氨表现出还原性和碱性 |
下列说法正确的是
| A.亚硫酸溶液中含有亚硫酸、水、二氧化硫三种分子 |
| B.用浓盐酸酸化高锰酸钾溶液,可增强高锰酸钾的氧化能力 |
| C.铵盐受热都易分解,生成氨和相应的酸 |
| D.SiO2是酸性氧化物,能与氢氧化钠溶液反应,不与任何酸反应 |