下列说法正确的是:
| A.摩尔是物质的量的单位 |
B.熔融状态下 或溶液中能导电的物质就是电解质 或溶液中能导电的物质就是电解质 |
| C.氧化还原反应的本质是化合价发生了变化 |
| D.得电子的物质被还原,是还原剂。 |
能够充分说明在恒温恒容下的密闭容器中,反应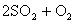

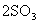 已达平衡状态的标志是()。
已达平衡状态的标志是()。
A.容器中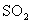 、 、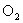 、 、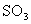 的物质的量之比为2:1:2 的物质的量之比为2:1:2 |
B.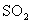 和 和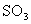 的物质的量浓度相等 的物质的量浓度相等 |
| C.反应容器内压强不随时间变化而变化 |
D.单位时间内生成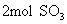 时,即生成 时,即生成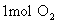 |
在一定温度下A(气)+3B(气)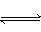 2C(气)达平衡的标志是( )
2C(气)达平衡的标志是( )
A.物质A、B、C的分子个数比为1:3:2
B.单位时间内生成A、C的物质的量之比为1:2
C.单位时间内生成A、B的物质的量之比为1:3
D.反应速率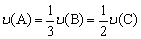
在容积固定的密闭容器中存在如下反应:A(g)+3B(g)  2C(g);△H<0
2C(g);△H<0
某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
下列判断一定错误的是()
| A.图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高 |
| B.图Ⅱ研究的是压强对反应的影响,且甲的压强较高 |
| C.图Ⅱ研究的是温度对反应的影响,且甲的温度较高 |
| D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高 |
可逆反应N2+3H2 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是()
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是()
| A.3v正(N2)=v正(H2) | B.v正(N2)=v逆(NH3) |
| C.2v正(H2)=3v逆(NH3) | D.v正(N2)=3v逆(H2) |
某温度下,在一容积可变的容器中,反应2A(g)+B(g) 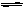 2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是()
2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是()
(A)均减半(B)均加倍(C)均增加1mol (D)均减小1mol