将H2、N2、O2三种气体分别放入三个不同的密闭容器中,当它们的温度、密度完全相同时,这三种气体的压强P的大小顺序是
| A.P(H2)>P(O2)>P(N2) | B.P(O2)>P(N2)>P(H2) |
| C.P(H2)>P(N2)>P(O2) | D.无法判断 |
“家庭小实验”是指利用家庭生活用品来进行的简单化学实验,下列实验不能成为“家庭小实验”的是()
| A.CO2不能支持蜡烛燃烧 | B.检验尿液中是否有葡萄糖 |
| C.除去热水瓶的水垢 | D.鉴别是羊毛织物还是化纤织物 |
下列有机物中,既能使溴水褪色,又能使酸性的KMnO4溶液褪色的是()
| A.乙烯 | B.苯 | C.甲烷 | D.乙酸 |
不溶于水,且密度小于水的是()
| A.苯 | B.乙酸 | C.四氯化碳 | D.溴苯 |
酯化反应是有机化学中的一类重要反应,下列对酯化反应理解不正确的是( )
| A.酯化反应是有限度的 | B.酯化反应可看成取代反应的一种 |
| C.酯化反应的产物只有酯 | D.浓硫酸可作酯化反应的催化剂 |
下列有关表达式中不正确的是()
A.乙烷的电子式: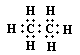 |
B.乙烯的结构式: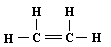 |
C.乙醇的结构式: |
D.乙酸的结构简式:CH3COOH |