在Na2SO4和Al2(SO4)3的混合溶液中,测得Al3+浓度为0.1mol/L,SO42-浓度为0.3mol/L,则混合溶液中Na+的浓度为( )
| A.0.15mol/L | B.0.45mol/L | C.0.6mol/L | D.0.3mol/L |
在常温下四个容积相同的抽空的密闭容器内,分别注入下列各组气体(先注入一种,再注入另一种),全部气体注入完毕后,容器中的压强从大到小的顺序是
①2mol氢气和1mol氧气 ②2mol硫化氢和1mol二氧化硫
③2mol一氧化氮和1mol氧气 ④2mol氨和lmol氯化氢
| A.①=②=③>④ | B.①>②=③>④ | C.③>④>①>② | D.①>③>④>② |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.在pH=1的溶液中:K+、Na+、SO42–、HCO3- |
B.在0.1 mol·L-1 Na2CO3溶液中:Al3+、K+、NO 、SO42– 、SO42– |
C.在0.1 mol·L-1 FeCl3溶液中:K+、NH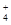 、I-、SCN- 、I-、SCN- |
D.在c( H+)/c(OH-)=10-12的溶液中:K+、Na+、ClO-、NO |
下列电子式书写正确的是
A.氯化钠 |
B.氨气 |
C.氯化钙 |
D.硫化钠 |
下列四个数据都表示合成氨的反应速率,其中代表同一反应速率的是
① = 0.3mol·L-1·min-1 ②
= 0.3mol·L-1·min-1 ② = 0.9 mol·L-1·min-1
= 0.9 mol·L-1·min-1
③ = 0.015 mol·L-1·s-1④
= 0.015 mol·L-1·s-1④ = 2.25 mol·L-1·min-1
= 2.25 mol·L-1·min-1
| A.①② | B.①③ | C.③④ | D.②④ |
原计划实现全球卫星通讯需发射77颗卫星,这一数字与铱(Ir)元素的原子核外电子数恰好相等,因此称为“铱星计划”.已知铱的一种同位素的质量数为191,则其核内的中子数与质子数之差是
| A.77 | B.114 | C.37 | D.268 |