Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如下,电解总反应为:2Cu+H2O Cu2O十H2↑。下列不正确的是
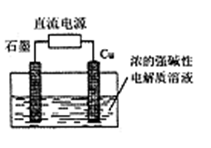
| A.石墨电极上产生氢气 |
| B.铜电极反应为:2Cu-2e-+2OH-Cu2O+H2O |
| C.铜电极接直流电源的正极 |
| D.当有0.1mol电子转移时,有0.1mol Cu2O生成 |
在恒温恒容的容器中进行下列反应:N2O4(g)  2NO2(g),若NO2的浓度由0.1mol/L增大到0.2mol/L时,需要5 s,那么NO2的浓度继续由0.2mol/L增大到0.4mol/L时,所需反应的时间为
2NO2(g),若NO2的浓度由0.1mol/L增大到0.2mol/L时,需要5 s,那么NO2的浓度继续由0.2mol/L增大到0.4mol/L时,所需反应的时间为
| A.小于10s | B.等于10s | C.大于10s | D.等于5s |
反应mA(s)+nB(g)  pC(g)△H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是
pC(g)△H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是
①m+n>p ②y点表示的正反应速率小于逆反应速率
③n>p ④x点比y点时的反应速率慢
⑤若降低温度,该反应的平衡常数增大
| A.①②⑤ | B.②④⑤ |
| C.只有①③ | D.①③⑤ |
下列变化过程,属于放热反应的是
①水蒸气变成液态水② 生石灰与水反应
③浓H2SO4稀释④ 醋酸电离
⑤Na投入水中 ⑥ 反应物的键能总和小于生成物的键能总和
| A.②③④⑤ | B.②⑤⑥ |
| C.②③④ | D.①②⑤⑥ |
下列反应符合图示的是
| A.酸碱中和反应 |
| B.Ba(OH)2·8H2O与NH4Cl晶体的反应 |
| C.黑火药爆炸 |
| D.用焦炭制水煤气 |
一定能反映化学平衡向正反应方向移动的是
| A.生成物的物质的量分数增大。 |
| B.v正 > v逆 |
| C.反应物浓度降低 |
| D.反应物的体积分数减少 |