下列叙述正确的是( )
| A.c(NH4+)相等的(NH4)2SO4溶液、(NH4)2Fe(SO4)2溶液和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2SO4]<c[(NH4)2Fe(SO4)2]<c(NH4Cl) |
| B.向AgCl悬浊液中滴入KI溶液,有AgI沉淀生成,说明AgCl的溶解度小于AgI的溶解度 |
| C.0.2 mol/L的NaHCO3溶液中c(H+)+c(H2CO3)=2c(CO32-)+c(OH-) |
| D.等体积、等物质的量浓度的Ba(OH)2、KOH和NH3·H2O三种溶液,将它们分别与V1 L、V2 L、V3 L等浓度的盐酸混合,若混合后溶液均呈中性,则V1>V2>V3 |
用图所示实验装置完成对应的实验(部分仪器已省略),能达到实验目的是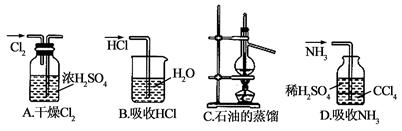
下列离子方程式正确的是
| A.向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO3-===3Fe3++NO↑+2H2O |
B.碳酸氢铵溶液与足量的NaOH溶液混合后加热: NH4++OH- NH3↑+H2O NH3↑+H2O |
| C.过量的KHSO4溶液与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-===BaSO4↓+H2O |
| D.向稀氢氧化钠溶液中通入少量CO2:OH-+CO2===HCO3- |
NA表示阿伏加德罗常数,下列叙述正确的是
| A.1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA。 |
| B.标准状况下,0.1 mol Cl2溶于水,转移电子的数目为0.1 NA。 |
| C.2.3 g Na与O2完全反应生成3.6 g产物时失电子数是0.1×6.02×1023 |
| D.标准状况下,11.2 L CH3CH2OH中含有的分子数为0.5NA |
下列变化一定属于化学变化的是
①工业制O2 ②爆炸 ③缓慢氧化 ④品红褪色 ⑤无水硫酸铜由白变蓝
⑥久置浓硝酸变黄 ⑦O2转化为O3 ⑧海水中提取金属镁
| A.①②③⑧ | B.④⑤⑥⑧ | C.③⑤⑥⑦⑧ | D.③④⑤ |
下列物质按纯净物、混合物、电解质、非电解质的顺序组合的一组为
| A.蒸馏水、氨水、乙醇、二氧化硫 | B.胆矾、空气、硫酸钠、干冰 |
| C.生铁、盐酸、浓硫酸、碳酸钙 | D.生石灰、漂白粉、氯化铜、硫酸钡 |