已知Zn(OH)2的溶度积常数为1.2×10-17(mol·L-1)3,则Zn(OH)2在水中的溶解度为( )
| A.1.4×10-6mol·L-1 | B.2.3×10-6mol·L-1 |
| C.1.4×10-9mol·L-1 | D.2.3×10-9mol·L-1 |
元素周期律的实质是( )
| A.相对原子质量逐渐增大 | B.核电荷数逐渐增大 |
| C.核外电子排布呈现周期性变化 | D.元素的化合价呈现周期性变化 |
1999年世界重大科技成果之一是超铀元素的发现,它有力地支持了“稳定岛”假说。原子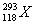 的中子数与电子数之差为( )
的中子数与电子数之差为( )
| A.0 | B.57 | C.118 | D.175 |
已知aAn+、bB(n+1)+、cCn-、dD(n+1)-是具有相同电子层结构的短周期元素形成的简单离子。下列叙述正确的是()
| A.原子半径:C>D>A>B |
| B.原子序数:b>a>d>c |
| C.离子半径:D>C>A>B |
| D.单质还原性:A>B>C>D |
饮用水的消毒剂有多种,其中杀菌消毒能力强且不会影响水质的理想消毒剂是()
| A.液氯 | B.漂白粉 | C.臭氧 | D.明矾 |
随着卤素原子半径的增大,下列递变规律正确的是( )
| A.单质的熔沸点逐渐降低 |
| B.卤素离子的还原性逐渐增强 |
| C.气态氢化物稳定性逐渐增强 |
| D.单质氧化性逐渐增强 |