常温下,用0.1000 mol/L NaOH溶液分别滴定20. 00 mL 0.1000 mol/L 盐酸和20. 00 mL 0.1000 mol/L 醋酸溶液,得到2条滴定曲线,如下图所示。若以HA表示酸,下列说法正确的是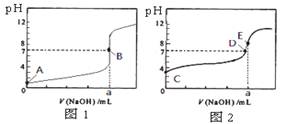
A.滴定盐酸的曲线是图2
B.达到B、D状态时,两溶液中离子浓度
均为c(Na+) = c(A—)
C.达到B、E状态时,反应消耗的n(CH3COOH)>n(HCl)
D.当0 mL< V(NaOH) <20. 00 mL时,对应混合溶液中各离子浓度由大到小的顺序均
为 c(A—) >c(Na+)> c(H+) > c(OH—)
下述实验操作不能达到实验目的的是
| 编号 |
实验目的 |
实验操作 |
| A |
验证SO2具有漂白性 |
将SO2通入品红溶液中,品红溶液褪色 |
| B |
验证Fe2+的还原性 |
FeCl2溶液中加入酸性KMnO4溶液,KMnO4溶液褪色 |
| C |
检验尿液中是否含有葡萄糖 |
在尿液中加新制的Cu(OH)2悬浊液加热至沸腾 |
| D |
验证Na2CO3溶液中存在水解平衡 |
在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去 |
下列关于有机物 的叙述不正确的是
的叙述不正确的是
| A.分子式为C6H10O |
| B.可发生加成、酯化和氧化反应 |
| C.分子中有两种官能团 |
| D.与HBr、溴水发生加成反应,产物都只有一种 |
氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一种反应物”在40℃~50℃时反应可生成它。CuH不稳定,易分解;CuH在氯气中能燃烧;跟盐酸反应能产生气体,以下有关的推断中错误的是
| A.“另一种反应物”一定具有还原性 |
| B.CuH既可做氧化剂也可做还原剂 |
| C.CuH+Cl2===CuCl+HCl(燃烧) |
| D.CuH+HCl===CuCl+H2↑(常温) |
能正确表示下列反应的离子方程式是
| A.硫酸铝溶液中加入过量氨水 Al3++3OH-= Al(OH)3↓ |
| B.碳酸钠溶液中加入澄清石灰水 Ca(OH)2+CO32-= CaCO3↓+2OH- |
| C.冷的氢氧化钠溶液中通入氯气 Cl2+2OH-= ClO-+Cl-+H2O |
| D.稀硫酸中加入铁粉 2Fe+6H+= 2Fe3++3H2↑ |
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.10gNH3含有4NA个电子 |
| B.0.1mol铁和0.1mol铜分别与0.1 mol氯气完全反应,转移的电子数均为0.2NA |
| C.标准状况下,22.4 L H2O中分子数为NA 个 |
| D.1L0.1mol·L-1Na2CO3溶液中含有0.1NA个CO32- |