用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,5.6L NO和5.6L O2混合后的分子总数为0.5NA |
| B.1mol Na2O2固体中含离子总数为4NA |
| C.7.1gCl2与足量NaOH溶液反应转移的电子数为0.2NA |
| D.在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10NA |
25℃时,在浓度均为1 mol/L的溶液中,各组离子一定能大量共存的是
| A.盐酸中:K+、Mg2+、Fe2+、MnO7-、 |
| B.NaOH溶液中:Cu2+、NH4+、SO42-、CO32- |
| C.FeCl3溶液中:Al3+、Na+、SCN-、SO42- |
| D.NaClO溶液中:K+、SO42-、OH-、NO3- |
煤气化过程中生成的CO和H2一定条件下制甲醇的反应如下:
CO(g)+ 2H2(g) CH3OH(g) △H < 0。其他条件不变,改变某一条件后,用示意图表示的反应变化正确的是
CH3OH(g) △H < 0。其他条件不变,改变某一条件后,用示意图表示的反应变化正确的是
| A |
B |
C |
D |
|
| 改变的条件 |
压强 |
温度 |
平衡体系增加H2 |
催化剂 |
| 变化的示意图 |
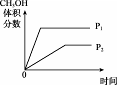 |
 |
 |
 |
假蜜环菌甲素可作为药物用于治疗急性胆道感染病毒性肝炎等疾病,其结构简式如下。下列对假蜜环菌甲素的性质叙述正确的是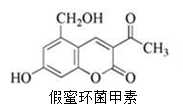
| A.假蜜环菌甲素可以发生消去反应 |
| B.1 mol假蜜环菌甲素可与 6 mol H2 发生加成反应 |
| C.假蜜环菌甲素可与 NaOH 溶液在加热条件下发生水解反应 |
| D.假蜜环菌甲素既能与Na反应生成H2,又能与NaHCO3反应生成CO2 |
下列叙述不正确的是
| A.植物油的不饱和程度高于动物油,植物油更易氧化变质 |
| B.除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、分液 |
| C.过氧化钠中含有离子键和非极性共价键,阴离子与阳离子的物质的量之比为1:1 |
| D.向某溶液中滴入稀盐酸产生使澄清石灰水变浑浊的气体,该溶液不一定含有CO32- |
解释下列操作或事实的离子方程式正确的是
A.把钠投入水中:2Na+2H2O 2Na+ + 2OH-+O2↑ 2Na+ + 2OH-+O2↑ |
B.把铜片放入氯化铁溶液中:Cu +Fe3+ Cu2+ +Fe2+ Cu2+ +Fe2+ |
C.铝制容器不能长期存放碱性食物:2Al + 2OH- 2AlO2-+ H2↑ 2AlO2-+ H2↑ |
D.向海带灰浸出液中加入硫酸、双氧水:2I-+2H++H2O2 I2+2H2O I2+2H2O |