X、Y、Z三种元素的原子,其最外层电子排布为ns1,3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是:
| A.X2YZ3 | B.X2YZ4 | C.XYZ2 | D.XYZ3 |
下列电子式书写正确的是()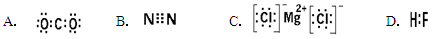
A、B、C均为短周期元素,它们在周期表中的位置如图.已知B、C两元素在周期表中族序数之和是A元素族序数的2倍;B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C 所在的一组是( )
A. O、P、Cl B. B、Mg、Si C. Be、Na、Al D. C、Al、P
下列化合物中阳离子与阴离子的半径比最小的是()
| A.LiF | B.KF | C.LiI | D.KI |
下列关于物质性质变化的比较中,不正确的是()
| A.离子还原性强弱:F->Cl->Br->I- | B.原子半径:Na>S>O |
| C.碱性强弱:KOH>NaOH>LiOH | D.酸性强弱:HClO4>H2SO4>H3PO4>H2SiO3 |
在元素周期表的金属与非金属的分界线附近可以寻找()
| A.稀有金属材料 | B.耐高温耐腐蚀的合金材料 |
| C.催化剂材料 | D.半导体材料 |