下列原子的外围电子排布式正确的是
| A.Zn:3d104s2 | B.Cr:3d44s2 | C.Ga:4s24p2 | D.S:3p4 |
某硫原子的质量是ag,12C原子的质量是bg,若NA只表示阿伏加德罗常数的数值,则下列说法中正确的是( )
①该硫原子的相对原子质量为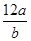
②mg该硫原子的物质的量为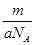 mol
mol
③该硫原子的摩尔质量是aNAg
④ag该硫原子所含的电子数为16NA
| A.①③ | B.②④ | C.①② | D.②③ |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A.11.2 L N2所含分子数为0.5NA |
| B.常温下,16 g CH4中共用电子对的数目为4NA |
| C.一定温度下,1 mol FeCl3水解生成NA个Fe(OH)3胶体颗粒 |
| D.在反应H2O2+Cl2=2HCl+O2中,每生成32 g氧气,转移4NA个电子 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A.同温同压下,原子数均为NA的氢气和氦气具有相同的体积 |
| B.84 g NaHCO3晶体中含有NA个阴离子 |
| C.标准状况下,11.2 L乙醇中含有0.5 NA个分子 |
| D.常温下,7.1 g Cl2与足量NaOH溶液作用,转移电子的数目为0.2 NA |
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A.5.6 g铁粉在0.1 mol氯气中充分燃烧,转移电子数为0.3NA |
| B.1 mol Na2O2与足量H2O充分反应,转移的电子数为2NA |
| C.7.8 g Na2O2中含有的阴离子数等于0.1NA |
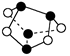
| D.0.5 mol雄黄(As4S4,结构如下图)中含有NA个S—S键 |
设阿伏加德罗常数为NA,标准状况下,mg N2和O2的混合气体含有b个分子,则ng该混合气体在相同状态下的体积为(单位为L)( )
A. |
B. |
C. |
D. |