下列说法正确的是( )
| A.pH=2与pH=1的硝酸中c(H+)之比为1:10 |
| B.Na2CO3溶液中c(Na+)与c(CO32-)之比为2:1 |
| C.0.2 mol?L-1与0.1mol/L醋酸中c (H+)之比为2:1 |
| D.NO2溶于水时,被氧化的n(NO2)与被还原的n(NO2)之比为3:1 |
一定量的盐酸跟过量的锌粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的 ①NaOH溶液 ②H2O ③CH3COONa固体 ④NaNO3溶液⑤稀硫酸
| A.②③ | B.②④ | C.②③④ | D.①②③④⑤ |
在 的平衡体系中,当分离出SO3 后下列说法中正确的是
的平衡体系中,当分离出SO3 后下列说法中正确的是
| A.正反应速率增大 | B.平衡常数增大 |
| C.正反应速率大于逆反应速率 | D.逆反应速率一直减小 |
在密闭容器中充入0.5mol N2和1.5mol H2发生反应: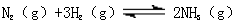
 ,充分反应后放出的热量为
,充分反应后放出的热量为
| A.等于92.4kJ | B.等于46.2kJ | C.大于46.2kJ | D.小于46.2kJ |
若将反应:Zn+H2SO4= ZnSO4+H2↑设计成原电池(如右图),则下列说法不正确的是
| A.该装置实现了化学能转化为电能 |
| B.b 极表面发生了还原反应 |
| C.c 溶液可以是ZnSO4溶液 |
| D.盐桥中的Cl-移向右边烧杯 |
下列说法不正确的是
| A.增大压强,活化分子百分数不变,化学反应速率增大 |
| B.升高温度,活化分子百分数增大,化学反应速率增大 |
| C.增大反应物浓度,活化分子百分数增大,化学反应速率增大 |
| D.使用催化剂,活化分子百分数增大,化学反应速率增大 |