标准状况下,m1g气体A与m2g气体B的分子数相等,下列说法中正确的是( )
A.1个A分子的质量是1个B分子的质量的 倍 倍 |
B.同温同体积的A与B的质量比为 |
C.同温同质量的A与B的分子数比为 |
D.同温同压下A与B的密度比为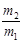 |
某有机物的结构如图,它不可能具有的性质是( )
| A.能跟NaOH溶液反应 | B.能使酸性KMnO4溶液褪色 |
| C.能发生酯化反应 | D.能发生水解反应 |
下列对有机物结构的叙述中不正确的是()
| A.硝基、羟基、甲基等都是官能团 |
| B.邻二氯苯不存在同分异构体说明苯分子中6个碳原子之间的键是完全一样的 |
| C.乙烯、苯分子中所有原子共平面 |
| D.CH2Cl2只有一种结构说明甲烷分子是正四面体结构,而不是平面正方形结构 |
关于实验室制备乙酸乙酯的说法中正确的是()
| A.实验前,先向试管中加入2mL浓硫酸,然后再加入3mL乙醇和2mL乙酸 |
| B.收集乙酸乙酯的试管中应加入的试剂为饱和碳酸钠溶液 |
| C.实验中需加入碎瓷片作催化剂 |
| D.导管末端要插入液面以下 |
在温度不变的条件下,密闭容器中发生如下反应:2SO2(g)+O2(g) 2SO3(g),
2SO3(g), 下列叙述能够说明反应已经达到平衡状态的是()
下列叙述能够说明反应已经达到平衡状态的是()
_
X原子的M电子层有2个电子;Y原子的M电子层比L电子层少1个电子;则X与Y 结合形成的化合物的化学式是()
结合形成的化合物的化学式是()
| A.XY2 | B.XY3 | C.XY | D.X2Y |