某同学按右图所示的装置进行电解实验。下列说法正确的是
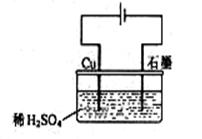
| A.电解过程中,铜电极上有H2产生 |
B.电解初期,主反应方程式为:Cu+H2SO4 CuSO4+H2↑ CuSO4+H2↑ |
| C.电解开始时,石墨电极上有铜析出 |
| D.整个电解过程中,H+的浓度不断增大 |
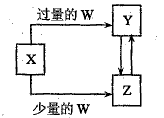
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是()
下列离子方程式书写不正确的是()
| A.苯酚钠溶液中通入少量二氧化硫: SO2+H2O+C6H5O-→C6H5OH+HSO3- |
| B.向碳酸氢铵溶液中加入过量的稀氢氧化钠溶液: NH4++HCO3-+2OH-=NH3·H2O+CO32-+H2O |
| C.向含有0.4mol FeBr2的溶液中通入0.3 mol Cl2充分反应 4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 |
| D.在AlCl3溶液中加入过量的氨水: |
Al3++3NH3·H2O=Al(OH)3↓+3NH4+
用固体二氧化钛(TiO2)生产海绵钛的装置图如下,其原理是在较低的阴极电位下,TiO2中的氧离子进入熔盐,阴极最后只剩下纯钛。下列说法中正确的是()
| A.当电路中有0.4 mol电子通过时,能产生2.24LO2 |
| B.通电后,O2-向阴极移动 |
| C.阴极的电极反应式为:TiO2+4e-=Ti+2O2- |
| D.石墨电极的质量不发生变化 |
在密闭容器中,对于可逆反应A(?)+3B(?) 2C(g)△H<0,平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是()
2C(g)△H<0,平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是()
A.当n(A):n(B):n(c)=1:3:2时,反应达到平衡状态
B.A、B聚集状态均无法确定
C.压强增大时,混合气体的平均相对分子质量增大
D.其他条件不变,升高温度,反应的平衡常数增大
下列实验现象预测正确的是()
| A.实验I:振荡后静置,上层溶液颜色保持不变 |
| B.实验Ⅱ:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 |
| C.实验Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 |
| D.实验IV:继续长时间煮沸,当光束通过体系时可产生丁达尔效应 |