同温同压下,两种气体的体积如果不相同,请你推测其主要原因是( )
A气体的分子大小不同 B气体的物质的量不同
C气体分子的化学性质不同 D气体分子间的平均距离不同
下列各组离子能大量共存,向溶液中通入足量相应气体后,各离子还能大量存在的是
| A.氯气:K+ Ba2+ SiO32— NO3— |
| B.二氧化硫:Na+ NH4+ HCO3— C1— |
| C.氨气:K+ Na+ AlO2— CO32— |
| D.甲醛:Ca2+ Mg2+ MnO4— NO3— |
下列说法不正确的是
| A.周期表中的碱金属元素,从上到下,熔点依次降低 |
| B.工业上精炼Cu,阳极用的电极材料是粗铜 |
| C.Fe3O4既能通过化合反应得到,又能通过置换反应得到 |
| D.二氧化硅能与NaOH溶液反应,又能和HF反应,属于两性氧化物 |
下列关于应用套管实验装置(部分装置未画出)进行的实验,叙述错误的是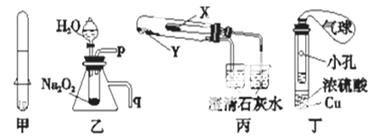
| A.利用甲装置可以制取少量H2 |
| B.利用乙装置可以验证Na2O2与水反应既生成氧气,又放出热量 |
| C.利用丙装置验证KHCO3和K2CO3的热稳定性,X中应放的物质是K2CO3 |
| D.利用丁装置制取SO2,并检验其还原性,小试管中的试剂可为酸性KMnO4溶液 |
实验室可用NaNO2+NH4Cl=NaCl+N2↑+2H2O制备N2,下列说法正确的是
| A.NaNO2发生氧化反应 |
| B.NH4Cl中的氮元素被还原 |
| C.N2既是氧化产物,又是还原产物 |
| D.每生成1mol N2转移电子的物质的量为6mol |
下列除去杂质的方法正确的是
| A.除去N2中的少量O2:通过灼热的CuO粉末,收集气体 |
| B.除 CO2中的少量HCl:通入饱和Na2CO3溶液,收集气体 |
| C.除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤 |
| D.除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤 |