在强酸性溶液中能大量共存的无色透明离子组是( )
A.K+、Na+、NO 、MnO 、MnO |
B.Mg2+、Na+、Cl-、SO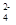 |
| C.K+、Na十、Br-、Cu2+ | D.Na十、Ba2+、OH-、SO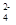 |
下列各选项所述的两个量中,前者一定小于后者的是
| A.纯水在25℃和100℃时的pH |
| B.在相同温度时,10mL0.1mol•L-1的醋酸溶液与100mL 0.01mol•L-1的醋酸溶液,由水电离出的c(H+) |
| C.用0.1mol•L-1NaOH溶液分别中和pH、体积均相同的醋酸和盐酸,所消耗NaOH 溶液的体积 |
| D.相同温度下,0.1mol•L-1的醋酸溶液和0.3mol•L-1的醋酸溶液中的电离平衡常数 |
常温下用pH试纸测定某溶液的pH,如果将pH试纸用蒸馏水润湿后,再把待测液滴到pH试纸上,跟比色卡对照,测得pH=6。则此溶液的实际pH
| A.小于6 | B.大于6 | C.等于6 | D.大于7 |
25℃时,在等体积的①pH=0的H2SO4溶液、②0.05mol/L的Ba(OH)2溶液、
③pH=10的Na2S溶液、④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是
| A.1∶10∶1010∶109 | B.1∶5∶5×109∶5×108 |
| C.1∶20∶1010∶109 | D.1∶10∶104∶109 |
已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+,要使溶液中
CH3COO-+H+,要使溶液中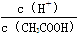 值增大,可以采取的措施是
值增大,可以采取的措施是
| A.加少量烧碱固体 | B.降低温度 |
| C.加少量冰醋酸 | D.加水 |
在下列叙述中,能论证盐酸是强酸,醋酸是弱酸的是
| A.将等体积pH=4的盐酸和醋酸稀释到pH=5的溶液,醋酸所加的水量少 |
| B.盐酸和醋酸都可用相应的钠盐和浓硫酸反应制取 |
| C.相同pH的等体积盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸pH变大,盐酸pH不变 |
| D.相同pH的盐酸和醋酸分别跟锌反应时,产生氢气的起始速率相等 |