2003年诺贝尔化学奖授予了美国科学家Peter Agre和Roderick Mackinnon以表彰他们在“水通道”和“离子通道”的研究成就。Mackinnon教授的研究内容主要是Na+、K+体积很接近,但在生物体内呈现的差别却高达1万倍,他革命性的让科学家观测Na+、K+在进入离子通道前、通道中以及穿过通道后的状态,可为病人在“离子通道”中寻找具体的病因,并研制相应药物。下列关于钠、钾的说法正确的是( )
| A.单质钠的密度比钾的密度小 | B.钠和钾在空气中燃烧的产物都是过氧化物 |
| C.钠和钾都是短周期元素 | D.钠和钾的合金[ω(K)=50%-80%]在室温下呈液态 |
化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂
HIn(红色溶液)  H+(溶液)+ In-(黄色溶液)
H+(溶液)+ In-(黄色溶液)
浓度为0.02 mol·L-1的下列各溶液:①盐酸②石灰水③NaCl溶液④NaHSO4溶液⑤NaHCO3溶液⑥氨水,⑦AlCl3溶液其中能使指示剂显红色的是
对于可逆反应:2A(g)+B(g) 2C(g) △H<0,下列各图正确的是
2C(g) △H<0,下列各图正确的是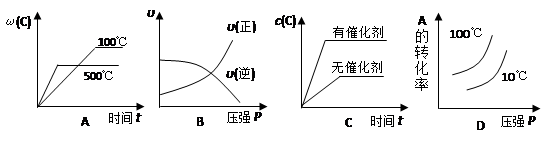
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得下图,则曲线a、b、c、d所对应的实验组别可能是
| 组别 |
c(HCl)(mol/L) |
温度(℃) |
状态 |
| 1 |
2.0 |
25 |
块状 |
| 2 |
2.5 |
30 |
块状 |
| 3 |
2. 5 |
50 |
粉末状 |
| 4 |
2.5 |
30 |
粉末状 |
A.4-3-2-1 B.1-2-3-4 C.3-4-2-1 D.1-2-4-3
下列关于热化学反应的描述中正确的是
| A.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol |
| B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)==2CO(g)+O2(g) △H=+566.0kJ/mol |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
已知:2Zn(s)+O2(g)=2ZnO(s)△H=-701.0kJ·mol-1
2Hg(l)+O2(g)=2HgO(s)△H=-181.6kJ·mol-1
则反应Zn(s)+ HgO(s)= ZnO(s)+ Hg(l)的△H为
| A.-519.4kJ·mol-1 | B.+259.7 kJ·mol-1 | C.-259.7 kJ·mol-1 | D.+519.4kJ·mol-1 |