X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核。通常状况下,W为无色液体。
已知:X+Y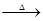 Z+W
Z+W
(1)Z的空间构型为 。
(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是 。
(3)1mol气态Z与O2反应生成液态W和一种由两种元素组成的气体物质,放出的热量为QkJ,写出该反应的热化学方程式: 。
(4)一定温度下,将1mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。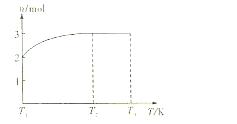
①温度在T1—T2之间,反应的化学方程式是: 。
②温度在T2—T3之间,气体的平均相对分子质量是(保留1位小数) 。
③若将实验所得的平衡 混和气体通入足量的水中,欲使气体被完全吸收则至少应同时通入标准状况下的空气 L。(设空气组成为:N2与O2,体积比4:1)
混和气体通入足量的水中,欲使气体被完全吸收则至少应同时通入标准状况下的空气 L。(设空气组成为:N2与O2,体积比4:1)
2009年8月,陕西省凤翔县长青镇马道口村和邻村孙家南头村的村民们自发到宝鸡各大医院检测发现,两村数百名婴幼儿及儿童绝大多数被检测出体内铅含量超标,其中部分超标严重,已达到中毒标准。两村民居南北环抱着的一家年产铅锌20万吨的冶炼企业,被疑与此有关。
(1)铅(原子序数为82)位于元素周期表的 周期 族,已知+2价铅比+4价铅稳定,+4价铅有较强的氧化性。将PbO2与浓盐酸加热反应产生黄绿色的气体,写出该反应的离子方程式 ,将SO2通入棕色PbO2的悬浊液中会产生白色沉淀,写出该反应的化学方程式 。
(2)铅锭冶炼厂采用火法冶炼铅,铅在自然界中以方铅矿(PbS)的形式存在,主要生产过程是先煅烧方铅矿制成PbO,再用CO还原PbO制备铅。上述生产过程中的主要化学方程式为 、 。
(3)铅蓄电池是典型的可充电型电池,它的正负极板是惰性材料,电池总反应式为: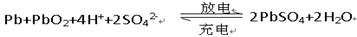 。放电时正极的电极反应式是 ;电解液中H2SO4的浓度将(填“变大”“变小”或“不变“);当外电路通过电子2mol时,理论上负极板的质量增加 g。
。放电时正极的电极反应式是 ;电解液中H2SO4的浓度将(填“变大”“变小”或“不变“);当外电路通过电子2mol时,理论上负极板的质量增加 g。
(4)铅在工业中应用广泛,如为了增强彩釉的亮度,陶瓷业在釉中常加入少量的铅。铅在酸性溶液中容易溶解,生成+2价铅进入人体,写出铅“吃醋”的化学方程式: 。汽车工业为提高发动机的使用寿命,常在汽油中加入抗震剂四乙基铅的分子式: 。
(7分)用乙醛还原新制备的Cu(OH)2可以生成红色的Cu2O沉淀。再加入过量的乙酸,使Cu2O发生歧化反应生成Cu2+和Cu,新生成的细小的晶体铜分散在溶液中即形成黄绿色透明铜溶胶。试写出表示以上反应过程的化学方程式。
(1) 。
(2) 。
(3)怎样证明新制得的分散系是胶体?
。
(7分)用乙醛还原新制备的Cu(OH)2可以生成红色的Cu2O沉淀。再加入过量的乙酸,使Cu2O发生歧化反应生成Cu2+和Cu,新生成的细小的晶体铜分散在溶液中即形成黄绿色透明铜溶胶。试写出表示以上反应过程的化学方程式。
(1)。
(2)。
(3)怎样证明新制得的分散系是胶体?
。
(10分)向胶体中加入少量电解质或将两种带相反电荷的胶体混合,能使胶体粒子聚集长大,形成的颗粒较大的沉淀从分散剂里析出,这个过程叫做聚沉。在Fe(OH)3胶体中,逐滴加入HI稀溶液,会产生一系列变化:
(1)先出现红褐色沉淀,原因是。
(2)随后沉淀溶解,溶液呈黄色,该反应的离子方程式为。
(3)最后溶液颜色加深,原因是。此反应的离子方程式为。
(4)用稀盐酸代替HI稀溶液,能出现上述哪些相同的现象(填序号)
。
(1)a与b应满足的关系是__________(写表达式)。
(2)a能否等于2?__________(填能、不能、无法确定)。
(3)a=3的硅酸盐的表达式_____________。
(以氧化物形式表示)