有一无色溶液,可能含有K+、Al3+、Mg2+、NH、Cl-、SO、HCO、MnO中的一种或几种。为确定其成分,进行如下实验:(1)取部分溶液,加入适量Na2O2固体,产生无色无味的气体并生成白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;(2)另取部分溶液,加硝酸酸化的Ba(NO3)2溶液,有白色沉淀产生。则此溶液中肯定存在的离子是
| A.K+、HCO、MnO | B.Al3+、Mg2+、HCO |
| C.Al3+、Mg2+、SO | D.Al3+、Mg2+、NH、Cl- |
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、HCO3-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如图所示,下列说法正确的是()
| A.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1 |
| B.ab段发生的离子反应为:Al3++3OH-= Al(OH)3↓,Mg2++2OH-= Mg(OH)2↓ |
| C.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+、Na+ |
| D.d点溶液中含有的溶质只有Na2SO4 |
往含0.2 mol KOH和0.1 mol Ca(OH)2的溶液中持续地通入CO2气体,当通入气体的体积为6.72 L(标准状况)时立即停止,则在这一过程中,溶液中离子的物质的量n和通入CO2的体积V的关系示意图正确的是(气体的溶解忽略不计) ( )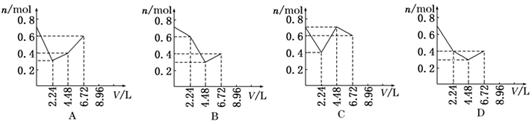
FeS与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO和H2O,当NO2、N2O4、NO的物质的量之比为1︰1︰1时,实际参加反应的FeS与HNO3的物质的量之比为()
| A.1∶6 | B.1∶7 | C.2∶11 | D.16∶25 |
下列叙述正确的是()
| A.浓度和体积相同的FeBr2、FeI2溶液中,分别通入少量氯气后都首先发生置换反应 |
| B.XCl3的溶液能与铜片发生反应,则铜的金属性一定比X强 |
| C.非金属X能将Fe氧化到+3价,但非金属Y不能,则Y的氧化性一定比X强 |
| D.Cl2和SO2等体积充分混合后,通入品红溶液,溶液颜色没有明显变化 |
标准状况下,某同学向100 mLH2S饱和溶液中通入SO2,所得溶液pH变化如图所示,下列分析中,正确的是( )
| A.ab段反应是:SO2+2H2S===3S↓+2H2O |
| B.亚硫酸是比氢硫酸更弱的酸 |
| C.原H2S溶液的物质的量浓度为0.05 mol/L |
| D.b点对应的溶液导电性最强 |